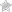Тромбоз и эмболия тромбофлебит
Патологическая анатомия / Пат.анатомия Тромбоз и Эмболия
Материалыдляподготовкикпрактическомузанятиюпотеме: «Тромбоз и эмболия»
1. Графылогических структур
4. Иллюстративный материал
7. Эталоныответовк тестовымзаданиям
1. ГРАФЫЛОГИЧЕСКИХСТРУКТУР ТРОМБОЗ
Сущность процесса: прижизненное свертывание крови в просвете сосудов или полостях сердца.
Условия, способствующие тромбообразованию:
1) общие – изменение состава и реологических свойств крови;
2) местные – изменение скорости и правильности кровотока, повреждение сосудистой стенки.
Механизмы образования тромба:
а) агглютинация тромбоцитов; б) коагуляция фибриногена; в) агглютинация эритроцитов;
г) преципитация белков плазмы.
Виды тромбов по составу:
а) белый (фибрин, тромбоциты, лейкоциты); б) красный (преобладание эритроцитов); в) гиалиновый (белки плазмы).
Виды тромбов по отношению к просвету сосуда:
а) обтурирующий; б) пристеночный; в) свободный.
Последствия: а) обтурирующего – венозное полнокровие, ишемия, некроз тканей, инфаркт; б) пристеночного – ишемия.
Исходы: а) асептический аутолиз; б) организация; в) канализация; г) петрификация; д) септический аутолиз; е) отрыв, превращение в эмбол.
Сущность процесса: перенос током крови или лимфы частиц, не встречающихся в норме, и закупорка ими сосудов;
Виды эмболий по виду эмбола: а) тромбоэмболия; б) микробная; в) тканевая, клеточная; г) жировая; д) воздушная; е) газовая; ж) инородными телами.
а) оторвавшиеся тромбы из полостей сердца, артерий, вен; б) кучки микробов из очагов воспаления; в) кусочки тканей и группы клеток, опухолей;
г) капли жира при повреждении жировой клетчатки и трубчатых костей; д) воздух при ранении вен шеи, грудной клетки, малого таза; е) газы крови при форсированной декомпрессии; ж) инородные тела, попавшие в кровоток.
Последствия эмболий: остановка сердца при эмболии легочной артерии (тромбоэмболия), некрозы, инфаркты, кровоизлияния в органах (тромбоз, эмболия жировая, воздушная), образование метастазов опухолей (тканевая эмболия), генерализация инфекции, метастатические гнойники (частички инфицированных тромбов), микробная эмболия, кессонная болезнь (газовая эмболия), острая легочная недостаточность, остановка сердца (жировая, воздушная).
• Стаз (от лат. stasis — остановка) — резкое замедление и остановка тока крови в сосудах микроциркуляторного русла, главным образом в капиллярах.
Причиной развития стаза являются нарушения циркуляции крови, возникающие при действии физических (высокая и низкая температура) и химических (токсины) факторов, при инфекционных,
инфекционно-аллергических и аутоиммунных заболеваниях, болезнях сердца и сосудов.
Механизм развития. В возникновении стаза большое значение имеют изменения реологических свойств крови, обусловленные развитием сладж-феномена (от англ. sludge — тина), для которого характерно прилипание друг к другу эритроцитов, лейкоцитов или тромбоцитов и нарастание вязкости плазмы, что приводит к затруднению перфузии крови через сосуды микроциркуляторного русла. Развитию внутрикапиллярной агрегации эритроцитов способствуют следующие факторы:
— изменения капилляров, ведущие к повышению их проницаемости и плазморрагии;
— нарушение физико-химических свойств эритроцитов;
— изменение вязкости крови за счет грубодисперсных фракций белков;
— нарушения циркуляции крови — венозное полнокровие (застойный стаз); — ишемия
(ишемический стаз) и др.
Стаз — явление обратимое. Длительный стаз ведет к необратимым гипоксическим изменениям —
некробиозу и некрозу.
Тромбоз (от греч. thrombosis — свертывание) — прижизненное свертывание крови в просвете сосуда или полостях сердца. Образующийся при этом сверток крови называют тромбом. Хотя тромбоз представляет собой один из важнейших механизмов гемостаза, он может стать причиной нарушения кровоснабжения органов и тканей с развитием инфарктов, гангрены. Патогенез. Патогенез тромбоза
складывается из участия как местных, так и общих факторов. К местным факторам относят изменения
сосудистой стенки, замедление и нарушение тока крови. Среди изменений сосудистой стенки особенно важно повреждение внутренней оболочки сосуда, чаще всего обусловленное атеросклеротическими и воспалительными поражениями ее. К повреждению стенки сосуда ведут и ангионевротические расстройства — спазмы артерий и артериол. Повреждение эндокарда при эндокардитах, инфарктах миокарда также сопровождается тромбообразованием. Замедление и нарушение (завихрение) тока крови
в артериях обычно возникают вблизи атеросклеротических бляшек, в полости аневризмы, при спазме; в венах — при варикозном расширении. Роль нарушений тока крови в развитии тромбоза подтверждается наиболее частой их локализацией на месте ветвления сосудов. О значении замедления тока крови для тромбообразова-ния свидетельствует частое возникновение тромбов в венах при развитии сердечнососудистой недостаточности, при сдавлении вен опухолями, беременной маткой, иммобилизации
конечности. К общим
факторам патогенеза тромбоза относят нарушение регуляции свертывающей и
систем крови и изменение состава крови. Главная роль принадлежит
нарушениям баланса между свертывающей и противосвертывающей системами в регуляции жидкого
состояния крови в сосудистом русле: Состояния повышенной свертываемости (гиперкоагуляция) часто являются следствием обширных хирургических операций и травм, беременности и родов, некоторых лейко-юв, сопровождающихся тромбоцитозом (истинной полицитемии и других миелопролиферативных заболеваний), спленэктомии, эндотоксемии, шока, реакций гиперчувствительности, злокачест-венных опухолей.
Среди изменений состава (качества) крови наибольшее значение имеет повышение вязкости. Оно может быть обусловлено эритроцитозом или полицитемией, возникающими при дегидратации (чаще у детей), при хронических гипоксических состояниях (дыхательной недостаточности, цианотических врожденных пороках сердца), истинной полицитемии, увеличении содержания грубодисперсных фракций белков (например, при миеломной болезни).
С практической точки зрения важно выделить группы больных со склонностью к образованию тромбов. К ним можно отнести:
• больных, находящихся на длительном постельном режиме после операции;
• страдающих хронической сердечно-сосудистой недостаточностью (хроническим венозным полнокровием);
• больных с атеросклерозом;
• онкологических больных; — беременных;
• больных с врожденными или приобретенными состояниями гиперкоагуляции,
предрасполагающими к рецидивирующему тромбозу.
Механизм образования тромба. Инициальным моментом тромбообразования является повреждение эндотелия. Тромб образуется при взаимодействии тромбоцитов (кровяных пластинок), поврежденного эндотелия и системы свертывания крови (коагуляционного каскада).
Тромбоциты. Основная их функция — поддержание целости сосудистой стенки — направлена на прекращение или предотвращение кровотечения и является важнейшим звеном гемостаза. Тромбоциты осуществляют следующие функции:
• участвуют в репарации эндотелия посредством выработки PDGF (тромбоцитарный фактор роста);
• формируют тромбоцитарную бляшку на месте повреждения сосуда в течение нескольких минут — первичный гемостаз;
• участвуют в коагуляционном каскаде (вторичный гемостаз) путем активации фактора 3
тромбоцитов, что в конечном счете приводит к тромбообразованию.
Эндотелий. Для сохранения крови в своем обычном состоянии необходима целостность (структурная и функциональная) сосудистого эндотелия. Интактная эндотелиальная клетка модулирует некоторые звенья гемостаза и обеспечивает тромбо-резистентность, т.е. противостоит тромбообразованию в результате следующих процессов:
• продукция гепарансульфата — протеогликана, активирующего антитромбин III, который нейтрализует тромбин и другие факторы свертывания, включая IXa, Xa, XIa и ХIIа;
• секреция естественных антикоагулянтов, таких как тканевый активатор плазминогена; — расщепление АДФ;
• инактивация и резорбция тромбина;
• синтез тромбомодулина — поверхностноклеточного протеина, связывающего тромбин и превращающего его в активатор протеина С — витамин К-зависимый плазменный протеин, который ингибирует коагуляцию, лизируя факторы Va и VI—IIа;
• синтез протеина S — кофактора активированного протеина С;
• продукция PGI-2 — простациклина, обладающего антитромбогенным эффектом;
• синтез оксида азота (II) (NO), который действует аналогично PGI-2.
Понимание этих антитромбогенных механизмов, осуществляемых эндотелиальной клеткой на ее поверхности, позволяет понять значение дисфункции эндотелия как триггера тромбообразования.
Существуют также следующие факты, доказывающие протромбогенную функцию эндотелия:
• эндотелий синтезирует фактор Виллебранда, который способствует агрегации тромбоцитов и фактора V;
• эндотелий способен связывать факторы IX и X, что может вызвать коагуляцию на поверхности эндотелия;
• под воздействием интерлейкина-1 и фактора некроза опухоли (ФНО) эндотелий выбрасывает в
плазму тромбопластин — потенциальный инициатор свертывания крови по внешней системе (внешнему пути).
Активация системы свертывания крови. Это решающий этап в прогрессировании и стабилизации тромба. Процесс завершается образованием фибрина — вторичный гемостаз. Это многоэтапный каскадный ферментативный процесс— коагуляционный каскад, требующий довольно много времени; при этом последовательно активируются проферменты. В процессе свертывания прокоагулянты — тромбопластины, превращаются в активные ферменты — тромбины, способствующие образованию из циркулирующего в крови растворимого фибриногена нерастворимого фибрина. Образующиеся нити фибрина скрепляют агрегаты тромбоцитов, образовавшиеся при первичном гемостазе. Это имеет большое значение для предотвращения вторичного кровотечения из крупных сосудов, наступающего через несколько часов или дней после травмы.
Механизм тромбообразования (тромбогенез) представлен следующими звеньями.
1. Адгезия тромбоцитов к обнаженному коллагену в месте повреждения эндотелиальной выстилки осуществляется с помощью фибронектина на поверхности тромбоцитов и стимулируется в большей степени коллагеном типа III, чем коллагеном базальной мембраны (IV тип). Медиатором является фактор Виллебранда, вырабатываемый эндотелием.
2. Секреция тромбоцитами АДФ и тромбоксана-А 2 (Тх-А 2 ). вызывающего вазоконстрикцию и агрегацию тромбоцитов (блокирование образования Тх-А 2 небольшими дозами аспирина лежит в основе превентивной терапии тромбообразования), гистамина, серотонина, PDGF и др.
3. Агрегация тромбоцитов — образование первичной тромбоцитарной бляшки.
4.Активация процесса свертывания крови, или коагуляционного каскада осуществляется с помощью следующих механизмов: внутренней системы свертывания, которая запускается контактной активацией фактора XII (Хагемана) коллагеном, фактора XI, прекалликреина, высокомолекулярного кининогена и усиливается фосфолипидом тромбоцитов (фактор 3), высвобождающимся при конформационных изменениях их мембраны; внешней системы свертывания, которая запускается тканевым тромбопластином, высвобождающимся из поврежденного эндотелия (тканей), и активирует фактор VII. В конечном итоге оба пути приводят к превращению протромбина (фактор II) в тромбин (фактор Па),
который способствует превращению фибриногена в фибрин, а также вызывает дальнейшее выделение АДФ и Тх-А 2 из тромбоцитов, способствуя их агрегации.
5. Агрегация стабилизируется образующимися отложениями фибрина — стабилизация первичной бляшки. В дальнейшем фибриновый сверток захватывает лейкоциты, агглютинирующиеся эритроциты и преципитирующие белки плазмы крови.
Таким образом, можно выделить следующие стадии морфогенеза тромба:
• коагуляция фибриногена с образованием фибрина;
• преципитация плазменных белков.
Система свертывания работает в тесной связи с фибринолитической системой, которая модулирует коагуляцию и препятствует тромбообразованию. Механизм действия фибринолитической системы складывается из следующих стадий:
1. превращение проэнзима плазминогена в плазмин — наиболее важный фибринолитический фермент;
2. растворение фибрина с помощью плазмина;
3. взаимодействие фибринолитической системы с системой свертывания на уровне активации фактора XII в ХПа связывает систему свертывания, систему комплемента и кининовую
Морфология тромба. Тромб обычно прикреплен к стенке сосуда в месте ее повреждения, где начался процесс тромбообразования. Он может быть пристеночным (т.е. закрывать только часть просвета) или обтурирующим. Поверхность тромба шероховатая. Пристеночные тромбы в крупных артериях могут иметь гофрированную поверхность, что отражает ритмичное выпадение склеивающихся тромбоцитов и выпадение фибрина при продолжающемся кровотоке. Тромб, как правило, плотной консистенции, сухой.
В зависимости от строения и внешнего вида, что определяется особенностями и темпами тромбообразования, различают белый, красный, смешанный (слоистый) и гиалиновый тромбы.
Белый тромб состоит преимущественно из тромбоцитов, фибрина и лейкоцитов, образуется медленно при быстром токе крови (чаще в артериях). Красный тромб, помимо тромбоцитов и фибрина, содержит большое число эритроцитов, образуется быстро при медленном токе крови (обычно в венах). В наиболее часто встречающемся смешанном тромбе, который имеет слоистое строение (слоистый тромб) и пестрый вид, содержатся элементы как белого, так и красного тромба. В смешанном тромбе различают головку (имеет строение белого тромба), тело (собственно смешанный тромб) и хвост
(имеет строение красного тромба). Головка прикреплена к эндотелиальной выстилке сосуда, что отличает тромб от посмертного сгустка крови. Слоистые тромбы чаще образуются в венах, в полости
аневризмы аорты и сердца. Гиалиновый тромб — особый вид тромбов, образующихся в сосудах микроциркуляторного русла; он редко содержит фибрин, состоит из разрушенных эритроцитов, тромбоцитов и преципитирующих белков плазмы, напоминающих гиалин. Увеличение тромба происходит путем наслоения тромботических масс на первичный тромб, причем рост тромба может происходить как по току крови, так и против тока.
Исход тромбоза. Может быть различен. Кблагоприятным исходам относят асептический аутолиз
тромба, возникающий под влиянием протеолитических ферментов и прежде всего плазмина. Установлено, что большинство мелких тромбов рассасывается в самом начале их образования. Другим благоприятным исходом является организация тромба, т.е. замещение его соединительной тканью, которая может сопровождаться процессами канализации и васкуляризации (восстановление проходимости сосуда). Возможно обызвествление тромба, в венах при этом возникают камни — флеболиты.
К неблагоприятным исходам относят отрыв тромба с развитием тромбоэмболии и септическое расплавление тромба, которое возникает при попадании в тромботические массы гноеродных бактерий, что приводит к тромбобактериальной эмболии сосудов различных органов и тканей (при сепсисе).
Значение тромбоза. Определяется быстротой его развития, локализацией и распространенностью. Обтурирующие тромбы в артериях — явление опасное, так как приводят к развитию инфарктов и гангрены.
• Эмболия (от греч. emballon — бросать внутрь) — циркуляция в крови (или лимфе) не встречающихся в нормальных условиях частиц и закупорка ими сосудов. Сами частицы называются эм-
Эмболы чаще перемещаются по току крови — ортоградная эмболия:
— из венозной системы большого круга кровообращения и правого сердца в сосуды малого круга;
— из левой половины сердца и аорты и крупных артерий в более мелкие артерии (сердца, почек, селезенки, кишки и др.).
В редких случаях эмбол в силу своей тяжести движется против тока крови — ретроградная эмболия. При наличии дефектов в межпредсердной или межжелудочковой перегородке возникает парадоксальная эмболия, при которой эмбол из вен большого круга, минуя легкие, попадает в артерии большого круга кровообращения. В зависимости от природы эмболов различают тромбоэмболию, жировую, воздушную, газовую, тканевую (клеточную), микробную эмболию и эмболию инородными
Тромбоэмболия — наиболее частый вид эмболии, возникает при отрыве тромба или его части. Тромбоэмболия легочной артерии. Это одна из наиболее частых причин внезапной смерти у
больных в послеоперационном периоде и больных с сердечной недостаточностью. Источником тромбоэмболии легочной артерии при этом обычно являются возникающие при венозном застое
тромбы вен нижних конечностей, вен клетчатки малого таза. В генезе смерти при тромбоэмболии легочной артерии придается значение не столько механическому фактору закрытия просвета сосуда, сколько пульмонокоронарному рефлексу. При этом наблюдается спазм бронхов, ветвей легочной артерии и венечных артерий сердца. При тромбоэмболии мелких ветвей легочной артерии обычно развивается геморрагический инфаркт легкого.
Артериальная тромбоэмболия. Источником артериальной эмболии чаще являются пристеночные тромбы, образующиеся в сердце: тромбы в левом предсердии при стенозе левого атриовентрикулярного отверстия (митральный стеноз) и фибрилляции; тромбы в левом желудочке при инфаркте миокарда; тромбы на створках левого предсердно-желудочкового (митрального) и аортального клапанов при ревматических, септических и других эндокардитах, пристеночные тромбы, возникающие в аорте в случае атеросклероза. При этом наиболее часто возникают тромбоэмболия ветвей сонной артерии, средней мозговой артерии (что приводит к инфаркту мозга), ветвей мезентериальных артерий с развитием гангрены кишки и ветвей почечной артерии с развитием инфаркта почки. Часто развивается тромбоэмболический синдром с инфарктами во многих органах.
Жировая эмболия развивается при попадании в кровоток капель жира. Обычно это происходит в случае травматического повреждения костного мозга (при переломе длинных трубчатых костей), подкожной жировой клетчатки. Изредка жировая эмболия возникает при ошибочном внутривенном введении масляных растворов лекарственных или контрастных веществ. Попадающие в вены жировые капли обтурируют капилляры легких или же, минуя легкие, через артериовенозные анастомозы поступают в капилляры почек, головного мозга и других органов. Жировые эмболы обнаруживаются обычно только при микроскопическом исследовании срезов, специально окрашенных для выявления жиров (Суданом III). Жировая эмболия приводит к острой легочной недостаточности и остановке сердца, если выключается 2 / 3 легочных капилляров. Жировая эмболия капилляров мозга вызывает появление многочисленных точечных кровоизлияний в мозговой ткани; при этом возможен смертельный исход.
Воздушная эмболия развивается при попадании в кровоток воздуха, что изредка встречается при ранении вен шеи (этому способствует отрицательное давление в них), после родов или аборта, при повреждении склерозированного легкого, случайном введении воздуха вместе с лекарственным веществом. Попавшие в кровь пузырьки воздуха вызывают эмболию капилляров малого круга кровообращения, наступает внезапная смерть. На вскрытии воздушная эмболия распознается по выделению воздуха из правых отделов сердца при проколе их, если предварительно заполнить полость перикарда водой. Кровь в полостях сердца имеет пенистый вид.
Газовая эмболия характерна для кессонной болезни, развивается при быстрой декомпрессии (т.е. быстром переходе от повышенного к нормальному атмосферному давлению). Высвобождающиеся при этом пузырьки азота (находящегося при высоком давлении в растворенном состоянии) вызывают закупорку капилляров головного и спинного мозга, печени, почек и других органов. Это
сопровождается появлением в них мелких фокусов ишемии и некроза (особенно часто в ткани мозга). Характерным симптомом являются миалгии. Особая склонность к развитию кессонной болезни отмечается у тучных людей, поскольку большая часть азота задерживается жировой клетчаткой.
Тканевая эмболия возможна при разрушении тканей в связи с травмой или патологическим процессом, ведущим к поступлению кусочков тканей (клеток) в кровь. К тканевой относят также эмболию амниотической жидкостью у родильниц. Такая эмболия может сопровождаться развитием синдрома диссе-минированного внутрисосудистого свертывания и привести к смерти. Особую категорию тканевой эмболии составляет эмболия клетками злокачественной опухоли, так как она лежит в основе метастазирования опухолей.
Микробная эмболия возникает в тех случаях, когда циркулирующие в крови микробы обтурируют просвет капилляров. Это могут быть также грибы, паразиты, простейшие. Часго бактериальные эмболы образуются при гнойном расплавлении тромба — тромбобактериальная эмболия. На месте закупорки сосуда бактериальными эмболами образуются метастатические гнойники.
Эмболия инородными телами наблюдается при попадании в кровь осколков металлических предметов (снарядов, пуль и пр.). К эмболии инородными телами относят также эмболию известью и кристаллами холестерина а геросклеротических бляшек, выкрашивающихся в просвет сосуда при их изъязвлении.
Значение эмболии. Для клиники значение эмболии определяется видом эмбола. Наибольшее значение имеют тромбоэмболические осложнения и прежде всего тромбоэмболия легочной артерии, ведущая к внезапной смерти. Велико также значение тромбоэмболического синдрома, сопровождающегося множественными инфарктами и гангреной. Не меньшее значение имеет бактериальная и тромбобактериальная эмболия — одно из ярких проявлений сепсиса, а также эмболия клетками злокачественных опухолей как основа их метастазирования.
Многие из видов нарушений кровообращения патогенетически тесно связаны и находятся в причинно-следственных отношениях, например связь кровотечения, плазморрагии и отека с полнокровием, связь малокровия с эмболией и тромбозом, а последнего — со стазом и венозным полнокровием. Расстройства кро-нообращения лежат в основе многих клинических синдромов, таких как острая и хроническая сердечная (сердечно-сосудистая недостаточность, диссеминированное внутрисосудистое свертывание крови (ДВС-синдром), тромбоэмболический синдром, шок.
• Шок — циркуляторный коллапс, сопровождающийся гипоперфузией тканей и снижением их оксигенации.
Причины шока. Различают следующие причины шока:
• снижение сердечного выброса, что обычно бывает при кровопотерях или тяжелой (левожелудочковой) сердечной недостаточности;
• распространенная периферическая вазодилатация, что наблюдается чаще при сепсисе или тяжелой травме, сопровождающейся гипотензией.
Типы шока и их патогенетические особенности. Различают гиповолемический, кардиогенный, септический и сосудистый типы шока.
Гиповолемический шок,в основе которого лежит циркуляторный коллапс, обусловлен острым уменьшением объема циркулирующей крови. Наблюдается при следующих состояниях:
• массивной потере плазмы поврежденной кожей (при обширных ожогах или травме, аллергических повреждениях кожи);
• потере жидкости и электролитов желудочно-кишечным трактом при тяжелой рвоте и диарее. Кардиогенный шок возникает вследствие снижения сердечного выброса при быстром падении
сократительной функции миокарда (при обширном инфаркте миокарда и других состояниях, приводящих к острой сердечной недостаточности).
Септический (токсико-инфекционный) шок может быть эндотоксическим (вызывается липополисаха-ридами, наиболее часто возникает при инфекциях, вызванных грамотрицательной микрофлорой) и экзотоксическим (при инфекциях, вызванных грамположительной микрофлорой, например экзотоксином Staphylococcus aureus).
Выделяют следующие звенья патогенеза септического шока: — эндотоксин и другие бактериальные продукты индуцируют освобождение производных арахидоновой кислоты и цитокинов (таких, как интерлейкин-1 и ФНО) в больших концентрациях; — стимулируется NO-синтетаза в эндотелии и гладких мышечных клетках сосудистой стенки, что сопровождается синтезом оксида азота (II) — NO, вызывающего стойкие вазодилатацию и гипотензию; а активируется система комплемента с освобождением анафилатоксинов С3а/С5а; — активация нейтрофилов приводит к повреждению эндотелия и резкому повышению проницаемости капилляров; активация фактора XII запускает процесс свертывания, что приводит к развитию ДВС-синдрома.
Сосудистый шок может быть анафилактическим и нейрогенным, который чаще всего связан с тяжелой травмой (травматический шок). Пусковым механизмом нейрогенного шока является афферентная (преимущественно) болевая импульсация, что приводит к реактивной периферической вазодилатации.
Развитие сосудистого шока связано с «секвестрацией крови» (в крупных периферических сосудах благодаря потере вазомоторного тонуса и в капиллярах вследствие постоянной венулярной констрикции), увеличением сосудистой проницаемости, с замедлением кровотока вследствие развития сладж-феномена.
Тромбоз и эмболия
Тромбоз
Тромбозом называется прижизненное свертывание крови или лимфы в просвете сосуда с частичной или полной закупоркой его просвета, ведущей к нарушению кровотока. Образующийся при этом сгусток крови или лимфы называется тромбом.
Тромбоз возникает при различных инфекциях и интоксикациях, после операций, при атеросклерозе, наклонности сосудов к спазмам (гипертоническая болезнь), застое крови в венах, воспалительных и аутоаллергических процессах в сосудах и тканях (ревматизм) и т. д.
В эксперименте тромбообразование можно наблюдать под микроскопом на прозрачных перепонках, например на препарате расправленной брыжейки лягушки. Около стенки небольшой вены кладут кристаллик поваренной соли, приводящей к повреждению сосуда. В поврежденном сосуде ток крови замедляется, периферический плазматический слой кровяного столба становится уже, в нем появляются в большем по сравнению с нормой количестве лейкоциты и тромбоциты. Последние задерживаются на поврежденном участке сосуда, склеиваются друг с другом и сливаются в одну гомогенную бесцветную или слегка зернистую массу. К этой массе по периферии пристают в большем или меньшем количестве и лейкоциты — образуется так называемый агглютинационный или белый тромб. Повреждение эндотелия сосудов сопровождается выходом тканевого тромбопластина в кровь. Там он активируется проконвертином и переводит протромбин крови в тромбин. Тромбин вызывает быструю агрегацию тромбоцитов и их лизис. Тромбоциты в присутствии Са ++ способствуют новому, массивному образованию тромсопластина. Далее в присутствии Са ++ и при участии фибриназы (XIII-фактора) образуются нити фибрина, заполняющие просвет поврежденного сосуда. В этих нитях задерживаются, застревают эритроциты — образуется коагуляционный тромб. Постепенно увеличиваясь, тромб может закрыть просвет сосуда и прекратить кровоток.
Патогенез тромбообразования. Тромбообразованию способствуют следующие факторы: замедление тока крови, повреждение стенок кровеносного сосуда и изменения свертывающей системы крови.
Замедление тока крови. Роль замедления тока крови в тромбообразовании подтверждается тем, что:
- а) в венах, где скорость тока крови меньше, чем в артериях, гораздо чаще образуются тромбы;
- б) тромбы преимущественно возникают в таких участках венозной системы, где ток крови особенно медленный (венозные сплетения таза, вены нижних конечностей);
- в) тромбы чаще развиваются в местах патологического расширения сосудов (в аневризмах, варикозно расширенных венах);
- г) тромбы нередко возникают при ослаблении сердечной деятельности (особенно в пожилом возрасте).
Однако в эксперименте не удается вызвать тромбообразование при одном лишь замедлении кровотока. Так, если с большой осторожностью, не повреждая сосудистую стенку, перевязать крупный кровеносный сосуд с двух концов, то кровь в таком изолированном сосуде долго сохраняется в жидком виде. Следовательно, одного лишь застоя крови недостаточно для образования тромба.
Повреждение стенок кровеносных сосудов. Известно, что в эксперименте повреждение стенок сосудов легко вызывает тромбоз. Патоморфологические наблюдения также подтверждают это положение: тромбы легко возникают на атероматозных язвах артерий, в местах перевязок сосудов, при воспалительных их изменениях, при инфекционно-токсическом поражении внутреннего слоя сосудистой стенки или клапанов сердца, при эндокардитах и пр.
В нормальном состоянии внутренняя поверхность сосудов покрыта тонким, постоянно обновляющимся слоем фибрина, уменьшающим вязкость крови и смачиваемость эндотелия сосудов кровяной плазмой. Фибринная пленка обладает также антикоагулянтными свойствами, предотвращающими свертывание крови на ее поверхности. В здоровом организме нет условий для образования фибрина в количествах, достаточных для тромбоза сосудов, так как избыток фибрина быстро лизируется фибрино-литической системой. Однако, если на внутренней стенке сосуда откладывается возрастающее количество фибрина, его антикоагулянтные свойства уменьшаются и, наоборот, нарастает смачиваемость сосудистой стенки. В силу этого увеличиваются поверхностные силы притяжения между эндотелием и форменными элементами крови, особенно слабозаряженными тромбоцитами.
Свертывающая система крови. Процесс тромбообразования зависит от состояния тромбоцитов крови и динамического равновесия между факторами свертывающей системы крови и фибринолитической системой.
Силам поверхностной активности тромбоцитов, определяющим их особую .«клейкость» и способность легко осаждаться и склеиваться, противостоит их отрицательный поверхностный потенциал, благодаря которому тромбоциты удерживаются во взвешенном состоянии. Заряд тромбоцитов может меняться в зависимости от ряда условий (например, он уменьшается при нарастании в крови слабоотрицательно заряженных глобулинов (—8—12 мкв) или почти лишенного заряда фибриногена (—3—5 мкв) и при сдвиге — кислотно-щелочного равновесия в кислую сторону. При ряде заболеваний число тромбоцитов крови повышается, а устойчивость их уменьшается. Осаждение и склеивание тромбоцитов сопровождается их разрушением и освобождением из них целого ряда биологически активных веществ, в том числе участвующих в процессе свертывания крови (ускоритель превращения протромбина в тромбин, ускоритель превращения фибриногена в фибрин, ингибитор гепарина — антигепариновый фактор) и др.
Внутрисосудистое свертывание крови и образование тромбов могут возникнуть при уменьшении антикоагулянтной активности крови (снижении содержания антикоагулянтов или увеличении активности их ингибиторов) или увеличении в крови коагулянтов (тромбин, тромбопластин). В опытах на животных установлено, что внутривенное введение тромбина, тромбопластина, тканевых экстрактов, некоторых бактериальных эндотоксинов, змеиных ядов и др. вызывает внутрисосудистое свертывание крови. Введение больших доз этих веществ обусловливает массивное тромбообразование и приводит к гибели животных. При этом свертывание крови возникает без нарушений интимы сосудов и замедления кровотока.
Внутрисосудистое свертывание крови не всегда ведет к образованию тромбов, так как возникающий фибрин поглощается ретикулоэндотелиальными клетками и быстро лизируется фибринолитической системой.
Ослабление фибринолитической активности способствует возникновению тромбов. Так, прием больших количеств жира ускоряет свертывание крови и одновременно понижает фибринолитическую активность. То же наблюдается как при экспериментальном атеросклерозе, так и у больных с атеросклерозом, инфарктом миокарда.
Сочетание повышенной склонности к свертыванию крови с ослаблением ее фибринолитической активности характеризует претромботическое состояние, которое может при соответствующих условиях (изменения стенок сосудов, спазм) привести к тромбозу.
Последствия тромбозов. В результате тромбозов могут возникать тромбофлебиты и тромбартерииты, флеботромбозы, тромбоэмболическая болезнь.
Тромбофлебиты и тромбоартерииты — воспаление вены или артерии, сопровождающееся тромбозом. Ведущим фактором тромбообразования являются повреждения стенки сосудов. Низкая фибринолитическая активность крови и сниженная антикоагулянтная активность ее, характерные для тромбофлебитов, способствуют росту тромбов.
Флеботромбозы — первичный тромбоз вен преимущественно нижних конечностей. Тромбы возникают при этом в результате изменения свертывающей системы крови (ослабление фибринолитической и антикоагулянтной активности крови, усиление агглютинации тромбоцитов).
Существенное значение имеет замедление кровотока. Флеботромбозы возникают в послеоперационном и послеродовом периодах, а также при массивных травмах сосудов. Тромбы при этом не прикреплены к стенке сосудов, что может вести к эмболиям.
Клинические проявления тромбоза кровеносных сосудов или полостей сердца с нередким заносом тромбоэмболов в другие участки сердечно-сосудистой системы называется тромбоэмболической болезнью. За последние десятилетия частота тромбоэмболической болезни значительно возросла. Основными причинами этого считаются:
- а) малоподвижный образ жизни, особенно жителей больших городов, способствующий застою крови;
- б) увеличение среди населения числа ожиревших и пожилых лиц, особенно склонных к тромбозам;
- в) резкое сокращение инфекционной заболеваемости и смертности, а в связи с этим увеличение контингента лиц пожилого возраста, подвергающихся тяжелым хирургическим операциям, сложному медикаментозному лечению и т. п.
Эмболия
Эмболией называется закупорка кровеносных и лимфатических сосудов частицами, занесенными током крови или лимфы и обычно не встречающимися в крови. Переносимые частицы называются эмболами.
Эмболы бывают эндо- и экзогенного происхождения. Чаще встречаются эндогенные эмболы. По механизму образования различают следующие виды эндогенных эмболов:
Тромбоэмболия — отрыв от места образования и занос в кровеносные сосуды кусочков тромбов. Легко отрываются частицы тромбов, образовавшихся на клапанах сердца, где условия переноса этих тромбов в большой или малый круг кровообращения особенно благоприятны.
Очень опасна эмболия сосудов мозга, возникающая в результате отрыва пристеночных тромбов, образовавшихся в крупных артериях.
Тканевая и клеточная эмболия возникает в тех случаях, когда группы клеток заносятся из одного органа в другой током крови, например эмболия ветвей легочной артерии клеточными элементами печени при травме печени, синцитиальными клетками последа, частицами клапанов сердца при язвенном их распаде. Возможна эмболия клеточными элементами опухолей (один из механизмов метастазирования).
Жировая эмболия — капельки жира поступают в кровеносную систему из ткани, богатой жиром, например после перелома длинных трубчатых костей или размозжения жировой клетчатки.
Жировые эмболы заносятся в легкие и через артерио-венозные анастомозы и легочные капилляры в большой круг кровообращения. Отсюда возможна жировая эмболия капилляров головного мозга, почечных клубочков и др.
Из экзогенных эмболов наибольшее значение имеют воздушная и газовая эмболии.
Воздушная эмболия — закупорка кровеносных сосудов пузырьками воздуха, попавшими в вены из окружающей атмосферы. Велика опасность воздушной эмболии при ранениях крупных вен (верхняя полая, яремная, подключичная), где вследствие присасывающего действия грудной клетки создается отрицательное давление. Кроме того, стенки этих вен фиксированы прилежащей костной тканью либо фасциями, поэтому они плохо спадаются. Проникающий в ток крови воздух попадает в правый желудочек, где может образоваться большой воздушный пузырь, тампонирующий полости правого сердца и препятствующий поступлению в них крови из большого круга кровообращения. Часть воздуха в виде мелких пузырьков проникает в сосудистую сеть легкого, что может быстро привести к смертельному исходу.
Разновидностью воздушной эмболии является газовая эмболия, возникающая, например, при кессонной болезни. Резкий перепад барометрического давления (быстрый подъем водолаза с большой глубины, разгерметизирование кабины самолета или скафандра на большой высоте) вызывает быстрое освобождение растворенных в крови под большим давлением газов.
Среди экзогенных эмболий хотя и редко, но наблюдаются эмболии конгломератами бактерий или паразитов из какого-либо очага инфекции или занос трихин из кишечника в легкое через лимфатические сосуды и грудной лимфатический проток. Описаны случаи эмболии инородными телами во время ранений, например осколками пуль и снарядов.
Направление движения эмболов определяется направлением тока крови. Перенос эмболов возможен по трем основным направлениям:
- 1) в сосуды малого круга кровообращения (эмболы заносятся из венозной системы большого круга и правого сердца;
- 2) в сосуды большого круга кровообращения (эмболы заносятся из левого сердца, артериальной системы большого круга и изредка из легочных вен);
- 3) в систему воротной вены печени (эмболы заносятся из многочисленных ветвей воротной вены брюшной полости).
Особый случай представляют ретроградная и парадоксальная эмболии.
При ретроградной эмболии эмбол в силу тяжести и расстройства общего кровообращения спускается вниз в направлении, обратному току крови, например из нижней полой вены — в вены нижних конечностей или почечную вену и т. п.
Ретроградному движению эмболов способствует повышение внутри-грудного давления при резких выдохах, например при кашле или сдавлении грудной клетки.
Парадоксальная эмболия возникает при наличии дефектов в межпредсердной и межжелудочковой перегородках сердца. Тогда эмболы, приносимые током венозной крови в правое сердце, попадают сразу в левое сердце (минуя систему легочных сосудов) и оттуда — в артериальную систему.
Последствия эмболии. Они зависят от места заноса эмболов. Здесь, кроме механического затруднения поступления крови и местных расстройств кровообращения (ишемия), имеют большое значение патологические рефлексы, возникающие из местных тканевых и сосудистых хеморецепторов, на другие сосудистые области. Раздражителями для этих рецепторов могут служить как сам эмбол, так и местные гипоксия и ацидоз. В начальной фазе эмболии раздражение рецепторов кровеносных сосудов приводит к мобилизации защитно-приспособительных реакций oрганизма. К таковым при эмболиях в малом круге можно отнести тахикардию, одышку, раскрытие капилляров и расширение сосудов малого круга, спазм вен и артерий большого круга, кровообращения. Все эти реакции возникают рефлекторно: сам эмбол раздражает рецепторы легочных сосудов и в то же время затрудняет опорожнение правого желудочка, что повышает давление в правом предсердии и устьях полых вен — включается рефлекс Бейн—Бриджа. В результате закупорки легочных сосудов поступление крови в левое сердце уменьшено; следовательно, падает давление в аорте — возбуждаются аортальные и синокаротидные рецепторы и т. д.
А. Б. Фохт изучал эмболию малого круга кровообращения в опытах на животных путем внутривенного введения им взвеси ликоподия. Если после введения ликоподия перерезать блуждающие нервы на шее, эмболия протекает более благоприятно. Очевидно, это связано с устранением потока импульсов в центральную нервную систему с периферических рецепторов.
Характер функциональных расстройств при эмболии в большом круге кровообращения более разнообразен, чем при эмболии малого круга, в зависимости от того, какой сосуд закупорился эмболом. Нередко эмболия приводит к тяжелым функциональным расстройствам и смерти (например, при закупорке коронарных артерий или артерий головного мозга).
Инфаркт
Инфаркт (oт лат. infarciere — набивать, наполнять) — участок ткани, омертвевший в результате прекращения кровоснабжения. Инфаркт может возникнуть в результате тромбоза, эмболии или длительного спазма питающей артерии.
Инфаркты легче возникают в тех органах, в которых артерии имеют мало анастомозов или эти анастомозы оказываются недостаточными для развития коллатерального кровообращения, особенно если имеются общие расстройства кровообращения, например ослабление сердечной деятельности с застойными явлениями в органах.
В механизме развития инфарктов ведущее значение имеют ишемия и последующая гипоксия окружающих участок инфаркта тканей. Ишемия и последующая гипоксия подверженных инфаркту тканей приводят к резким расстройствам трофики — окислительно-восстановительных процессов, и накоплению в тканях продуктов межуточного обмена, биологически активных аминов и других веществ. В результате этого возникают функциональные расстройства сосудистой стенки (повышается проницаемость, меняется тонус и т. д.) и возбудимости периферических нервных образований. Так бледная окраска так называемого «белого инфаркта» зависит от того, что в результате ишемии возникает рефлекторный спазм сосудов окружающих инфаркт тканей. Это влечет за собой вытеснение крови не только из участка инфаркта, но и из окружающих тканей. Спазм препятствует также поступлению крови в участок инфаркта по анастомозам.
Белый инфаркт чаще возникает там, где недостаточно развиты коллатерали, например в селезенке, сердце, мозге, почках.
В эксперименте белый инфаркт можно получить путем перевязки веток коронарных артерий или почечной артерии.
В других случаях некротические участки пропитываются, «нафаршировываются» кровью, поступающей сюда из соседних вен. Такие инфаркты называются красными, или геморрагическими. В данном случае имеет значение изменение функционального состояния сосудистой стенки — расширение и повышение ее проницаемости вследствие воздействия продуктов тканевого распада.
Геморрагические инфаркты обычно возникают в легких, в кишечнике, иногда в головном мозге.
Следует учитывать также, что возникновению инфарктов способствуют общие расстройства организма — сердечная недостаточность и замедление кровотока в периферических сосудах, склонность тонической мускулатуры сосудов к длительным и повторным спазмам, например при коронарной болезни, нарушения жиро-липоидного обмена с повышением в крови бета-липопротеидов при атеросклерозе, и. наконец, нарушения в свертывающей системе крови. Так, например, почвой, на которой развивается инфаркт миокарда, нередко являются атеросклеротические поражения сосудов, которые подготавливаются и усиливаются предшествующей гипертонической болезнью. Как для атеросклероза, так и для гипертонической болезни III и II стадий свойственно повышение тромбо-образующих свойств крови (ускорение свертываемости крови, повышение тромбопластиновой активности, снижение свободного гепарина и угнетение фибринолиза).
Тромбозы и эмболии симптомы
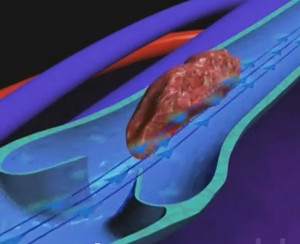 Тромбозы чаще образуются в венах. Причинами тромбоза могут быть заболевания, ведущие к изменению реактивности организма и к физико-химическим сдвигам в крови. Способствуют тромбозу повреждение сосудистой стенки, замедление кровотока и изменения в свертывающей системе крови. Оторвавшиеся участки тромба называются эмболами. Они могут закупорить сосуд, тогда говорят об эмболии. Чаще венозный тромб закупоривает легочные артерии. Кроме того, эмболию могут вызвать воздух и капли жира, попавшие в сосуд.
Тромбозы чаще образуются в венах. Причинами тромбоза могут быть заболевания, ведущие к изменению реактивности организма и к физико-химическим сдвигам в крови. Способствуют тромбозу повреждение сосудистой стенки, замедление кровотока и изменения в свертывающей системе крови. Оторвавшиеся участки тромба называются эмболами. Они могут закупорить сосуд, тогда говорят об эмболии. Чаще венозный тромб закупоривает легочные артерии. Кроме того, эмболию могут вызвать воздух и капли жира, попавшие в сосуд.
В настоящее время выявлено более 30 генов, мутации в которых предрасполагают к тромбозу. Наиболее важное значение придают гену протеина С (*176860, 2q13-q14, гена PROC). Гетерозиготность по его мутантным формам у больных с тромбозами выявляют в 10-25 раз чаще, чем в среднем в популяции (при гомозиготности развивается молниеносная пурпура новорождённых, обычно с летальным исходом). У гетерозиготных носителей дефектных генов к 60-летнему возрасту тромбозы развиваются в 100% случаев, тогда как при отсутствии мутаций в гене протеина С тромбоз выявляют только в 30% случаев.
В настоящее время доказана важная роль в развитии тромбозов гипер-гомоцистеинемии. Последнюю считают независимым и существенным фактором риска развития артериальных и венозных тромбозов, а также атеросклеротического поражения коронарных, мозговых и периферических сосудов. В основе гипергомоцистеинемии лежат генетические дефекты, приводящие к нарушению синтеза белков-ферментов, участвующих в метаболизме гомоцистеина
При гипергомоцистеинемии происходит активация всех компонентов гемостаза — сосудистой стенки, тромбоцитарного и плазменного звеньев. Гомоцистеин обладает цитотоксическим действием на эндотелий, за счёт увеличения образования свободных радикалов, а также ингибирует циклооксигеназную активность в клетках эндотелия и тем самым уменьшает образование простациклина. В тромбоцитах гомо-цистеин нарушает метаболизм арахидоновой кислоты, увеличивая высвобождение тромбоксана А2, что в свою очередь ведёт к повышению адгезивных и агрегационных свойств тромбоцитов. Гомоцистеин также способен вызывать активацию фактора V. Все эти эффекты в конечном итоге изменяют баланс между свёртывающей и противосвёртывающей системами крови в пользу преобладания первой и тем самым увеличивают риск тромбоза.
Течение эмболии периферических артерий зависят от локализации и размеров эмбола. Возникает резкая боль, похолодание конечности, бледность кожи. При эмболии легочных артерий — резкая боль в груди, выраженная одышка, цианоз, быстро развиваются расстройства кровообращения, исчезает пульс, больной теряет сознание и наступает смерть.
Радикальной операцией является эмболэктомия, которая производится в сосудистом отделении. При эмболии легочных артерий, а также эмболии периферических артерий конечности проводят лечение гепарином, стрептазой, кислородотерапию, сердечнососудистыми средствами.
Тромбоз почечной вены
Тромбоз почечной вены — это необычное заболевание, которое заключается в образовании сгустка крови в одной или обеих венах, которые поставляют кровь из почек назад к сердцу. У детей болезнь может появиться внезапно и закончиться почечной недостаточностью и серьезной болезнью. У взрослых болезнь может не вызывать никаких симптомов. Во многих случаях сгустки крови могут также образоваться в легочной артерии, где сгусток, известный как эмбол, может вызвать боль в груди и одышку.
• У взрослых тромбоз почечной вены почти всегда является результатом нефротического синдрома, хотя есть и другие причины.
• Диарея с сильным обезвоживанием является наиболее распространенной причиной болезни у детей.
• Повреждение живота или нижней части спины может привести к тромбозу почечной вены.
• Злокачественные опухоли в почках, которые распространяются в почечную вену, могут привести к тромбозу почечной вены.
• Беременность или использование пероральных противозачаточных средств увеличивает риск заболевания.
• У взрослых часто нет никаких признаков, поскольку сгусток растет медленно.
• Боль, обычно умеренная, в нижней части спины и в боку. Может быть заметна кровь в моче.
• У детей: лихорадка и озноб; кровь в моче.
• Боль в груди, одышка, кашель, возможно с кровавой мокротой, обильное потоотделение, беспокойство и неравномерное сердцебиение из-за эмбола в легочной артерии.
Диагностика
• История болезни и физическое обследование.
• Почечная венография (введение контрастного вещества в почечную вену перед рентгеном), ультразвуковое обследование или магнитно-резонансное обследование могут быть выполнены, чтобы определить расположение сгустка крови.
• Могут быть прописаны стрептокиназа или урокиназа (ферменты), чтобы растворить сгустки крови в серьезных случаях тромбоза обеих почечных вен, связанных с острой почечной недостаточностью.
• Антикоагулянты могут быть прописаны для длительного применения, чтобы уменьшить риск образования тромбов в легочных и почечных венах.
• У детей, жизнь которых находится в опасности, может быть необходимо хирургическое удаление пораженной почки.
Профилактика
• Профилактическое использование лекарств против свертывания крови (типа варфарина) может быть рекомендовано пациентам с высоким риском развития болезни, которые имеют большое количество белка в моче.
• Обратитесь к врачу, если у вас появилась постоянная боль в нижней части спины,или в боку или если у вас имеется нефротический синдром и вы испытываете боль в груди и одышку.
Эмболия легочной артерии
Эмболия легочной артерии возникает, когда сгусток крови, который проходит через вены, блокирует легочную артерию, один из сосудов, которые поставляют кровь к легким, где она обогащается кислородом. В большинстве случаев сгусток крови (тромб) образуется в вене ноги вследствие тромбоза; другими обычными источниками являются правые камеры сердца. Часть или все оторвавшиеся тромбы могут быть перенесены в легочные артерии. Скопления злокачественных клеток, жира или пузырьков воздуха в крови также могут сформировать эмболы, хотя это происходит редко. Эмбол размещается в главной легочной артерии или в одной из меньших артерий, прерывая поток крови через часть легких.
Симптомы появляются внезапно; их сила зависит от размера и числа эмболов. Болезнь может быстро стать фатальной, если поражена достаточно большая часть легких одним большим эмболом или многими маленькими. Приблизительно один случай из 10 приводит к внезапной смерти. Критическим является первый час эмболии легочной артерии, поэтому больному должна быть оказана немедленная помощь; те, кто выжил в течение достаточного времени, чтобы быть госпитализированным и диагностированным, поправляются. Развитие болезни наиболее благоприятно у молодых пациентов. Эмболия легочной артерии значительно чаще наблюдается у женщин, чем у мужчин (в соотношении приблизительно два к одному).
• Сгусток крови, перемещающийся из вены ноги, является наиболее обычной причиной эмболии легочной артерии.
• Иногда воздушный пузырь или скопление злокачественных клеток, жира, бактерий или другой материал могут заблокировать легочную артерию.
• Факторы риска включают: беременность; недавнюю операцию; предшествующий сердечный приступ или инсульт; длительное нахождение в постели (например, при выздоровлении от болезни); тучность; курение; переломы кости, особенно бедра или костей ноги; рак, особенно легких, мозга, груди, или печени; и наличие в семье тромбоза вен, эмболии легочной артерии и болезней, приводящих к образованию тромбов.
• Люди с болезнью сердца, эмфиземой или хроническим бронхитом подвержены более высокому риску серьезных последствий от эмболии легочной артерии.
• Внезапное начало боли в груди; боль обычно острая и ухудшается при глубоком дыхании.
• Кашель, возможно с кровавой мокротой.
• Признак чрезвычайного положения: потеря сознания.
Диагностика
• История болезни и физическое обследование.
• Электрокардиограмма помогает исключить сердечный приступ и обнаружить признаки повышенного давления в легочных артериях или других серьезных сердечно-сосудистых заболеваний.
• Радиоизотопное сканирование, перед которым необходимо вдохнуть небольшое количество радиоактивного газа и ввести радиоактивные частицы в кровь, может выявить заблокированные части кровеносных сосудов в легких.
• Артериография легких (введение контрастного красителя в легочные артерии перед рентгеном) является единственным совершенно достоверным способом идентифицировать эмболию легочной артерии.
• Контрастная компьютерная томография используется, чтобы выявить обширную эмболию легки:
• Антикоагуляционные средства, например, гепарин и варфарин, используется, чтобы предотвратить образование дальнейших сгустков крови.
• Тромболитические средства (растворяющие тромбы), например, активатор тканевого плазминогена стрептокиназа или урокиназа, могут быть введены кровь, чтобы ликвидировать блокаду сосуда.
• Анальгетики используются, чтобы уменьшить боль.
• Кислород может подаваться через маску, а в серьезных случаях, через респиратор.
• Больному необходимо немедленное лечение, ecли у него подозревают эмболию легких. Немедленно операция может потребоваться, если больше тромб блокирует главную легочную артерию.
Профилактика
• Прописанный врачом эластичный бинт может помочь предотвратить глубокий тромбоз вен на ногах у тех, кто входит в группу риска. Старайтесь не скрещивать ноги, когда сидите, так как это способствует развитию тромбов.
• Регулярный прием аспирина может быть необходим, чтобы предотвратить появление тромбов у пациентов, входящих в группу риска.
• Антикоагулянт гепарин может быть прописан в низких дозах для постоянного приема, чтобы уменьшить вероятность образования сгустков крови у людей, входящих в группу риска (например, больных хронической венозной недостаточностью, застойной сердечной недостаточностью или тех, кто недавно перенес сердечный приступ), или у пациентов, которым предстоит операция. После операции таким пациентам следует вставать с постели и начать ходить как можно быстрее, чтобы кровообращение улучшилось.
• Вместо гепарина может использоваться другая форма этого лекарства, низкомолекулярный фракционированный гепарин. Его можно принимать периодически.
• Коумадин, еще один антикоагулянт, может быть прописан для постоянного применения, после того как будут сняты острые симптомы эмболии.
• Внимание! Вызовите «скорую помощь», если у вас или у кого-то в вашем присутствии началась внезапная сильная боль в груди и одышка, наряду предчувствием беды или ощущением страха. Кроме эмболии легких такие симптомы могут также означать сердечный приступ или обострение другого сосудистого заболевания.
• Внимание! Вызовите немедленно «скорую помощь», если кто-то неожиданно теряет сознание.
Источники: http://studfiles.net/preview/5792177/, http://spravr.ru/tromboz-i-emboliya.html, http://medn.ru/statyi/trombozy.html