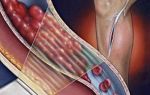
Тромбоз верхней полой вены у новорожденных
Тромбозы у новорожденных и недоношенных детей
Тромбозы у новорожденных и недоношенных детей.
Эпидемиология тромбозы у детей
Возрастной пик: самая высокая частота тромбозов у новорожденных и недоношенных детей (второй возрастной пик — пубертат).
Частота составляет 5/100 000 живорожденных.
У 24/10 000 новорожденных, получающих лечение в отделениях реанимации, развивается тромбоз.
Диагностика вытекает из клинических симптомов, сонографии, допплер-/дуплекс-сонографии, возможно флебо-/ангиографии, МРТ-ангиографии.
Причины тромбозы у детей
Врожденные причины (редко являются единственной причиной тромбозов):
Редко — дефицит ингибиторов: антитромбина, протеина С, протеина S.
Чаще — генетические дефекты:
- мутация фактора У-Лейдена-С1691 А, гетерозиготное или гомозиготное носительство
- мутация в гене протромбина-020210 А, гетерозиготное или гомозиготное носительство
- полиморфизм метилтетрагидрофоллатредуктазы (MTHFR-), гомозигота Т677Т.
- повышение липопротеинов (окончательный уровень устанавливается только после 1-го года жизни).
Приобретенные причины: центральный венозный катетер (тромбоз верхней полой вены), сердечный катетер, перипартальная асфиксия, шок, сепсис, полицитемия, пороки сердца, эксикозы, диабетическая фетопатия и антифосфолипидный синдром у матери.
Симптомы тромбозы у детей
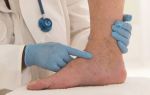
Венозные тромбозы: припухлость и синюшный цвет, иногда видны коллатерали.
Артериальные тромбозы: бледность, отсутствие пульса, невозможность измерить давление и сатурацию.
Центральный блок: например, приступ судорог.
Диагностика тромбозы у детей
Минимальная диагностика:
Общий анализ крови: гемоглобин, гематокрит, уровень тромбоцитов.
Коагулограмма: протромбиновый индекс, протромбиновое время, фибриноген, Д-димеры, (антитромбин).
Расширенная диагностика:
- может и должна проводиться в более поздние сроки.
- генетический анализ (дефекты, обозначенные): не ранее 2—3 дней после трансфузий. 1 мл крови в пробирку с ЭДТА. письменное согласие родителей.
- влияет на длительность реокклюзионной профилактики.
- зависимость показателей от возраста — необходим контроль в динамике.
Лечение тромбозы у детей
На сегодняшний день нет исследований, статистически доказывающих эффективность различных видов терапии.
Перед началом терапии обязательно выполнение нейросонографии.
Терапия выбора для новорожденных и недоношенных детей — гепаринизация.
При артериальных тромбозах должно обсуждаться вмешательство сосудистых хирургов (при периферических тромбозах это в большинстве случаев невозможно из-за недостаточной ширины сосудов и высокого Риска вазоспазма).
Обязательно привлечение гемостазиолога.
Тромболизис рекомбинантным активатором тканевого плазминогена или урокиназой
Внимание: всегда взвешивать необходимость и риск применения препарата!
- Жизнеугрожающие состояния (возможно также при синдроме верхней полой вены).
- Угрожающая потеря органа.
- Двусторонний тромбоз почечных вен (но: уровень эффективности при тромбозе почечных вен очень низкий, чаще — развитие «сморщенной почки», несмотря на результативный лизис).
- Угрожающая потеря конечности.
Внимание: тромбоз венозного синуса не является показанием для лизиса!
- Кровоизлияние в мозг (давностью менее 1 месяца).
- Операция или состояние после постановки центрального венозного катетера без возможности компрессии (
- 1
- 2
- 3
- 4
- 5
ПОБОЧНЫЕ ПРОЯВЛЕНИЯ ИНТЕНСИВНОЙ ТЕРАПИИ У НОВОРОЖДЕННЫХ
Кирилочев О.К., Нургалиев Р.И., Хазанов С.Н., Нураденова Г.Р., Морозов В.В.
Астраханская государственная медицинская академия,
Астрахань, Россия
Детская городская больница №1 (для новорожденных)В отечественной, да и зарубежной неонатологии проблемы, связанные с появлением «второй», ятрогенной болезни принято обходить молчанием. Ятрогения – это любое новое побочное заболевание, связанное с действиями врача, независимо от того, правильными или неправильными эти действия были. При возникновении ятрогений возможно и осуществлялись адекватные, правильно проведенные мероприятия, но особенности индивидуальной реактивности ребенка были таковы, что это способствовало осложнению. Следовательно, невозможно никакими способами смоделировать все методы интенсивной терапии, а значит необходимо выявлять и анализировать все издержки интенсивной терапии.
Цель работы: изучить возможные побочные явления при проведении интенсивной терапии у новорожденных за 19 лет работы отделения реанимации.
Под нашим наблюдением находилось 5 новорожденных с синдромом верхней полой вены в результате катетеризации подключичной вены. Симптоматика этого синдрома заключалась в появлении отечности верхней половины туловища, лица, головы. У 1 ребенка симптоматика отсутствовала, и заболевание при жизни не было диагностировано. В остальных случаях диагноз синдрома верхней полой вены был поставлен в 1, 2, 5, 13 сутки от возникновения первых симптомов, что было связано с маскировкой симптомами основного заболевания, изредка с недостаточной настороженностью в отношении этого синдрома при проведении катетеризации подключичной вены.
После возникновения тромбоза верхней полой вены следующим звеном патогенеза явился септический тромбофлебит, т.е. у всех новорожденных происходило инфицирование тромба на 5-12 день от катетеризации. Источником инфицирования была сопутствующая эндогенная или экзогенная бактериемия. При этом наиболее частым возбудителем оказался эпидермальный стафилококк. Известно, что гнойный флебит центральной вены – это эквивалент сепсиса, и в дальнейшем у детей происходило метастазирование с появлением новых гнойных очагов из-за гнойного расплавления тромба и его кумуляции. Следует отметить, что «легочный фильтр» в известной мере «смягчил» удар и поражались в основном правые отделы сердца и трехстворчатый клапан с развитием септического эндокардита (у 4-х детей). Метастатические поражения легких, почек в нашем наблюдении не отмечались. Для септического тромбофлебита как эквивалента сепсиса были характерны диффузно-дистрофические изменения паренхиматозных органов, прежде всего миокарда, печени, почек, гиперплазия селезенки («септическая селезенка»), лимфоузлов, которые выявлялись на секции.
Проанализировав эти наблюдения, мы убедились, что катетеризация подключичной вены может привести к развитию взаимно отягощающих заболеваний: синдрома верхней полой вены – септического тромбофлебита – сепсиса. Однако, при тщательном наблюдении «хронически катетеризированных» больных преимущества этого сосудистого доступа превышают риск осложнений.
Под нашим наблюдением находился 1 новорожденный ребенок, которому проводилась катетеризация пупочной вены, закончившаяся развитием пупочного сепсиса. В его пользу свидетельствовало то, что первичный септический очаг локализовался только в пупочной вене и из области пупочного кольца смещается в область ворот печени и внутрипеченочные сосуды. Наше внимание заслужило это наблюдение в связи с тем, что заболевание протекало в молниеносной форме. Катетеризация у доношенного ребенка была проведена в 1-е сутки жизни в родильном доме, на 3-и сутки отмечено катастрофическое ухудшение состояния с развитием ДВС-синдрома, гиповолемии, шока с летальным исходом на 5 сутки жизни.
На наш взгляд показанием для катетеризации пупочной вены у новорожденного могут быть только два – для проведения заменного переливания крови при гемолитической болезни новорожденных и для противошоковых мероприятий при тяжелой асфиксии. При этом важным условием должен быть срок нахождения катетера в пупочной вене – не более 48 часов.
Под нашим наблюдением находилось 15 новорожденных с бронхолегочной дисплазией (из них 12 — недоношенных), которым проводилась искусственная вентиляция легких (ИВЛ) в течение от 12 до 72 суток. Показанием для ИВЛ была дыхательная недостаточность, обусловленная врожденной пневмонией, аспирацией мекония, сепсисом, внутричерепным кровоизлияниям. Механическая вентиляция легких, токсическое действие кислорода вызвало множество отрицательных эффектов, которые привели к бронхолегочной дисплазии. Все новорожденные получили общепринятые методы терапии с включением бронходилататоров, мочегонных, стероидов и ИВЛ. Однако, учитывая широкую вариабельность причин бронхолегочной дисплазии у новорожденных, необходима дальнейшая оценка различных подходов в терапии этого заболевания.
Еще одной проблемой, связанной с интенсивной терапией и реанимацией, является нозокомиальная инфекция. При обследовании 26 новорожденных детей в динамике проведения ИВЛ у большинства из них выявлена смена флоры в трахеальных аспиратах. Колонизация нового возбудителя в дыхательных путях ребенка не зависела от генеза дыхательной недостаточности, которая была основанием для провидения ИВЛ, и сроков гестации. Постоянный мониторинг за эволюцией возбудителей в отделениях реанимации и интенсивной терапии позволит проводить соответствующие противоэпидемические мероприятия и целенаправленную антибиотикотерапию.
Таким образом, появление и рост побочных осложнений интенсивной терапии новорожденных до некоторой степени отражает цену, которую мы, а вернее новорожденный платит за научный прогресс. Совершенствование реаниматологов, неонатологов должно сопровождаться выявлением, анализом побочных проявлений интенсивной терапии. Внедрение новых методов, использование прежних традиционных методик диагностики и лечения должно происходить гласно, со скурпулезной оценкой не только пользы, но и вреда, так как любая терапия хороша настолько, насколько больной новорожденный этого заслуживает.
Внимание! Кафедра проводит первичную специализацию по анестезиологии-реаниматологии для отдельных категорий врачей!
Путевки на циклы можно заказать по телефону деканата 8-(812)-416-52-2516 авгста 2018 г.
В раздел «наука» — «план конференций» добавлена информация о Международном симпозиуме «Критические состояния у детей , который пройдет 25-27 сентября 2018 год в Санкт-Петербурге.12 марта 2018 г.
В разделе «Учеба» размещена информация о XI Международном образовательном курсе по регионарной анестезии «Белые Ночи регионарной анестезии» , который пройдет в Санкт-Петербурге 11 — 13 июня 20189 января 2018 г.
В раздел «Учеба» добавлен учебно-производственный план ФП и ДПО на 2018 год.10 мая 2017 г.
В раздел » публикации которые вы можете приобрести » добавлена новая книга » Позвоночно-спинномозговая травма у детей » Баиндурашвили А.Г., Виссарионов С.В., Александрович Ю.С., Пшениснов К.В.31 января 2017 г.
3-4 февраля 2017 года проводится Съезд анестезиологов и реаниматологов России. Дополнительная информация: Письмо замминистра Каграманяна И.Н. «16 января 2017 г.
В раздел «библиотека» выложен отсканированный вариант книги Гордеев В.И., Александрович Ю.С. Методы исследования развития ребенка: качество жизни (QOL) — новый инструмент оценки развития детей . — СПб, Речь 2001Тромбоз верхней полой вены у новорожденных
Выделяют следующие состояния, способствующие развитию тромбозов у новорождённых:
• аномалии сосудистой стенки (например, замедленное закрытие артериального протока) и её повреждения (прежде всего сосудистыми катетерами);
• расстройства (замедление) кровотока (например, при инфекциях; тяжёлой гипоксии, ацидозе);
• изменения реологических свойств крови (например, при поли- цитемии; тяжёлой дегидратации, гипоксии, врождённом дефиците антикоагулянтов).
Наиболее частые причины, вызывающие тромбозы у новорождённых:
• наличие сосудистых катетеров (особенно опасны артериальные катетеры);
• гипертромбоцитозы (например, при неонатальных кандидозах);
• шок и тяжёлое течение бактериальных и вирусных инфекций с вторичными васкулитами;
• антифосфолипидный синдром у матери;
Формирование тромбозов происходит также при ряде наследственных тромбофилических состояний:
• дефицит и/или дефекты физиологических антикоагулянтов (антитромбина III, протеинов С и S, тромбомодулина, ингибиторов внешнего пути активации свёртывания, кофактора II гепарина, активатора плазминогена), избыток ингибитора протеина С и/или ингибитора комплекса «антитромбин Ш-гепарин»;
• дефицит и/или дефекты прокоагулянтов [фактора V (Лейден), протромбина, плазминогена, фактора XII, прекалликреина, высокомолекулярного кининогена], а также тромбогенные дисфибриногенемии;
Клиническая картина
Клинические признаки тромбозов у новорождённых приведены в табл. 10-3.
Диагностика
При подозрении на тромбоз привлекают все диагностические средства для определения локализации тромба или исключения этой патологии. Используют различные варианты ультразвукового обследования, контрастной ангиографии.
Лечение тромбозов у новорождённых, предлагаемое разными авторами, достаточно противоречиво, поскольку в данном случае практически невозможны рандомизированные исследования и сделанные на их основе рекомендации с позиций доказательной медицины. Прежде всего, необходима коррекция факторов высокого риска развития тромбозов. При полицитемии выполняют кровопускание (10—15 мл/кг) с заменой выведенной крови фактором свёртывания крови VIII или изотоническим раствором натрия хлорида, назначают дезагреганты (никотиновую кислоту или пен- токсифиллин, пирацетам, аминофиллин, дипиридамол и др.). По возможности убирают сосудистые катетеры. При поверхностных тромбах кожу над ними смазывают гепариновой мазью4 (МНН: Гепарин натрия + Бензокаин + Бензилникотинат). К специальной антитромботической терапии прибегают редко. Для её выполнения чаще применяют гепарин натрия.
Таблица 10-3. Клиника тромбоэмболической болезни у новорождённых
Источники: http://www.sweli.ru/deti/do-goda/bolezni-detey-do-goda/trombozy-u-novorozhdennykh-i-nedonoshennykh-detej.html, http://www.airspb.ru/c_tez_18.shtml, http://for-medic.info/2010/12/trombozy/