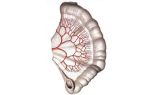
Тромбоз нижней полой вены при раке почки
Оперативное лечение больных раком почки с инвазией в нижнюю полую вену
Опухолевая инвазия нижней полой вены, являясь грозным осложнением, встречается в 3,5 — 9% случаев рака почки, прогноз при этом неутешительный.
Инвазия нижней полой вены опухолью в 50% случаев ничем не проявляется [Walsh, 1977; Esho, 1978]. Наличие первичной опухоли в почке еще не означает ее распространения в нижнюю полую вену. Однако имеются некоторые клинические проявления, которые могут дать повод подозревать это осложнение. К ним относятся:
- наличие варикоцеле, не исчезающего в положении лежа; если оно слева, то можно думать об инвазии как левой почечной, так и супраренальной части нижней полой вены, а если справа или с обеих сторон — то об обструкции последней;
- отеки нижних конечностей без венозной недостаточности в анамнезе (эти отеки вместе с протеинурией и гематурией дают все основания подозревать наличие опухолевой обструкции средней части нижней полой вены или тотального поражения последней);
- наличие расширенных вен передней брюшной стенки типа „головы медузы»;
- наличие синдрома Бадда-Киари, который развивается из-за прорастания опухоли в печеночные вены либо вторичного опухолевого тромбоза последних и выражается в боли в области печени, болезненной гепатомегалии, асците, желтухе и снижении функции печени;
- В редких случаях венокавальной обструкции, достигающей правого предсердия, может выслушиваться грубый систолический шум в третьем — четвертом межреберье слева и определяться признаки перегрузки правого предсердия на ЭКГ.
Диагностика. Поскольку клинические данные инвазии нижней полой вены опухолью недостаточны, ангиография остается единственным достоверным способом оценки состояния нижней полой вены. После уточнения диагноза опухоли почки при помощи артериографии, независимо от размеров опухолевого узла, обязательным является выполнение венокавографии. Опухолевая инвазия нижней полой вены венографически проявляется следующими признаками: 1) смещение нижней полой вены в противоположную от опухоли сторону; 2) краевое вдавление нижней полой вены; 3) сужение просвета нижней полой вены; 4) нечеткость контуров нижней полой вены; 5) наличие дефекта наполнения нижней полой вены с неровными зазубренными контурами; 6) окклюзия нижней полой вены; 7) наличие венозного рефлюкса по окольным венам.
Флотирующий опухолевый тромб может омываться контрастным веществом со всех сторон, и в таких случаях на венокавограммах он выявляется только ампулообразным расширением нижней полой вены выше места впадения почечной вены. Однако при этом на контуре нижней полой вены должна быть краевая „зарубка», соответствующая месту впадения тромба в просвет вены.
Прорастание опухолевого тромба в нижнюю полую вену вдоль почечной вены при относительно сохранном ее просвете распознается по характерной картине на венокавограммах — краевому дефекту наполнения стенки нижней полой вены в месте впадения в нее почечной вены при наличии венограммы этой почки.
Между размерами опухоли в почке и опухолевым тромбозом почечной и нижней полой вен не существует параллелизма, поэтому почечная флебография и венокавография должны обязательно выполняться при раке почки.
Таким образом, венографически можно определить верхнюю и нижнюю границу опухолевого тромба, выделить следующие виды его инвазии в нижней полой вене и соотношение последней с опухолью: 1) сдавление опухолью нижней полой вены или с интимным спаянйем с ее стенкой; 2) распространение опухоли вдоль почечной ножки с прорастанием стенки нижней полой вены; 3) инвазия в виде флотирующего опухолевого тромба; 4) смещенная опухолевая инвазия.
Каждый из этих видов опухолевой инвазии требует соответствующего оперативного пособия.
При раке правой почки со сдавлением опухолью нижней полой вены без или с интимным спаянйем с ее стенкой операция не представляет особой трудности. В связи с опасностью разрыва стенки нижней полой вены и кровотечения необходимо выделение вены вверх и вниз от места спаяния с опухолью. В случае повреждения вены разрыв ее зашивают непрерывным шелковым швом. В крайнем случае возможна перевязка нижней полой вены.
При распространении опухоли вдоль правой почечной ножки с прорастанием устья почечной вены и стенки нижней полой вены и при смещенной опухолевой инвазии выполняется краевая резекция нижней полой вены с последующим ее ушиванием.
Более распространенная опухолевая инвазия нижней полой вены по окружности или в проксимальном направлении не является препятствием к удалению опухоли, если в патологический процесс не вовлечено устье левой (противоположной) почечной вены или если последнее остается проходимым после ушивания проксимального конца нижней полой вены. В этом случае производится сегментарная резекция нижней полой вены.
Значительные трудности возникают в тех случаях, когда опухоль, прорастая вниз, достигает левой почечной вены так, что при ушивании культи нижней полой вены нарушается венозный отток из левой почки. В таком случае в зависимости от развития венозных коллатералей имеются два выхода из создавшегося положения: 1) при достаточном коллатеральном венозном оттоке, что устанавливается на операционном столе на основании сохраненной экскреторной функции при пережатии почечной вены, перевязывают левую почечную вену и производят резекцию нижней полой вены в требуемых масштабах; 2) при отсутствии или недостаточности коллатерального венозного оттока допустимые границы резекции нижней полой вены теоретически могут быть расширены благодаря использованию венозного аутотрансплантата, взятого из нижней полой вены ниже тромба; 3) при инвазии нижней полой вены в виде флотирующего тромба вначале выполняется временное прерывание кровотока в нижней полой вене для предупреждения миграции фрагментов опухолевого тромба, затем вскрывается нижняя полая вена и удаляется тромб, после чего ушивается дефект нижней полой вены.
Для прекращения венозного кровотока выше тромба нижняя полая вена выделяется по всей окружности (при необходимости перевязывается поясничная вена), пережимается выше и ниже впадения в нее почечных вен за пределами распространения тромба. Пережимаются также артериями вена левой почки. Необходимо отметить, что одно пережатие нижней полой вены не является достаточным. Следует перекрывать артерию почки, пораженной опухолью, специальным баллоном-катетером. При этом обескровливание почки и уменьшение ее размеров позволяют свободнее манипулировать на почечной и нижней полой венах и, таким образом, снизить риск фрагментации опухолевого тромба в этих сосудах.
При подобной тактике проблема удаления опухолевого тромба решается следующим образом: если опухолевый тромб заполняет почечную вену и лишь своим концом проникает в нижнюю полую вену, то для его удаления и ушивания венозной стенки достаточно применить зажим Сатинского.
Если опухолевый тромб внедрился в нижнюю полую вену и конец его находится выше впадения почечной вены, то накладывают турникеты на нижнюю полую вену выше левой и ниже правой почечных вен. Затем накладывают турнике ты на артерию и вену левой почки и «вскрывают нижнюю полую вену по ходу правой почечной вены, устье которой иссекают. Одним блоком удаляется почка, пораженная опухолью, почечная вена и опухолевый тромб из нижней полой вены. Дефект последней закрывается непрерывным шелковым или этиконовым швом.
Если опухолевый тромб распространяется до печеночных вен и выше, то лучше пользоваться торакоабдоминальным доступом в восьмом межреберье справа. При этой ситуации, чтобы достичь супраренальной части нижней полой вены, приходится пересечь правые треугольную и коронарную связки печени и пожертвовать соответствующими поясничными и нижними печеночными венами [McCullough, Git-tes, 1974]. Такая операция весьма травматична и нередко выходит за пределы компенсаторных возможностей организма больного.
При раке левой почки оперативное лечение больных с инвазией опухолевого тромба в нижнюю полую вену представляет весьма сложную проблему. В этом случае необходимо мобилизовать аорту, чтобы подойти и удалить необходимый участок нижней полой вены.
Для облегчения этого этапа операции предлагают пользоваться торакофренолюмбальным или торакоабдоминальным доступом. Эти операции травматичны, сопровождаются высокой летальностью (15%) и поэтому пока выполняются редко. При выполнении подобных операций следует избегать извлечения опухолевого тромба кюреткой, а Также наложения турникета на затромбированную вену с целью достижения прикавального сегмента почечной вены, чтобы максимально дальше ее перевязать. Эти приемы приводят к мобилизации, фрагментации и миграции опухолевого тромба.
Единственно правильной тактикой следует считать широкое выделение нижней полой вены в области впадения в нее почечных вен. Если опухолевый тромб входит в нижнюю полую вену, то необходимо наложить турникет на последнюю выше и ниже тромба, а при необходимости также на артерию и вену противоположной (правой) почки. Для предупреждения ретроградного тока крови по левой почечной вене и облегчения нефрэктомии целесообразно до операции окклюзировать или эмолизировать левую артерию. Остальной ход операции аналогичен операции на правой почке.
Хирург, выполняющий оперативное вмешательство на нижней полой вене, должен иметь в виду, что на долю ее инфраренальной части приходится 25 — 33% от сердечного венозного притока, на долю почечных вен — 25 % и печеночных вен также 25%. Поэтому при пережатии нижней полой вены на уровне правого предсердия резко снижается минутный объем сердца, что не происходит или мало меняется при пережатии нижней полой вены ниже печеночных вен.
После удаления опухолевой массы из нижней полой вены преднамеренно вызывают кровотечение из нее, которое способствует смыванию неудаленных фрагментов опухолевого тромба. Такой прием выполняется ну тем снятия турникета, наложенного на нижнюю полую вену ниже тромба при неснятом турникете выше тромба.
«Оперативная урология» — под редакцией академика АМН СССР Н. А. ЛОПАТКИНА и профессора И. П. ШЕВЦОВА
Тромбоз нижней полой вены при почечно-клеточном раке: вопросы реконструктивного хирургического лечения
Склонность рака почки- почечно-клеточного рака к распространению в виде тромба по почечной и нижней полой вене — одна из клинических характеристик данного заболевания, отмечаемая с частотой от 4 до 14%. Авторы провели лечение 942 пациентов по поводу рака почки. Тромбоз почечной и нижней полой вен по данным предоперационного обследования обнаружили у 104 (11,1%) пациентов. Оперировали 80 пациентов, при этом в 24 случаях провели резекцию фрагмента стенки нижней полой вены с тромбэктомией, в 7 — ушивание дефекта с применением заплаты. Летальность составила 6,25% при годичной выживаемости 90% и пятилетней 54,1%.
Ключевые слова: рак почки, тромбоз почечной, нижней полой вены, тромбэктомия.
Тромбоз нижней полой вены при почечно-клеточном раке: вопросы реконструктивного хирургического лечения
Злокачественные опухоли почки (в подавляю&щем большинстве случаев это рак) составляют 3,0-3,5% от общего числа злокачественных опухо&лей. В России ежегодно выявляют почти 9000 новых пациентов. Склонность почечно-клеточного рака к распространению в виде «опухолевого» тромба по почечной и далее по нижней полой вене (НПВ) — одна из клинических характеристик данного заболе&вания, отмечаемая с частотой от 4 до 14% [1-5]. Прогноз при раке почки достаточно неблагоприя&тен. При радикальном комплексном лечении специ&фичная по заболеванию пятилетняя выживаемость колеблется от 25 до 57% [6]. Хирургическое лечение остается основным методом, в задачи которого вхо&дит не только достижение онкологической ради&кальности, но и сохранение функции НПВ с одно&временным предотвращением тромбоэмболии ле&гочной артерии (ТЭЛА).
Несмотря на достаточный опыт, многие аспек&ты данной проблемы нуждаются в дальнейшем изу&чении. Обсуждаются биологические характеристики опухоли (помимо стадии), определяющие прогноз заболевания и тактику лечения, вопросы хирургического доступа, целесообразность искусственного и вспомогательного кровообращения, временных шунтов, оправданность операции при метастазах [7, 8].
Материал и методы
В отделениях Челябинского областного клини&ческого онкологического диспансера в течение по&следних 5 лет (по январь 2007 г.) проходили лечение по поводу рака почки 942 пациента в возрасте от 43 до 76 лет (в среднем 59,1 года). Мужчин было 58,3%, женщин — 41,7%. Проведенное всем больным ра&ком почки ультразвуковое исследование (УЗИ) од&новременно служило основным скрининговым ме&тодом диагностики тромбоза почечной и полой вен. Компьютерную томографию (Philips Tomoscan SR-5000, General Electric CT MAX 640) проводили при необходимости уточнения местной распростра&ненности процесса и для поиска отдаленных мета&стазов. В случае если исследование выполняют на современном аппарате в ангиографическом режиме, оно способно дать ответ на большинство вопросов по распространенности и характеру тромба.
Каваграфию проводили больным с подозрением на тромботическое поражение НПВ, уточняя разме&ры и локализацию тромба. При этом обязательным считали не только определение границ тромбоза и оценку его эмбологенности, но и визуализацию пе&ченочных вен при распространении патологиче&ского процесса в ретропеченочный сегмент НПВ (рис. 1).
Сосудистая инвазия опухоли по данным пред&операционного обследования обнаружена у 104 (11,1%) пациентов. Из них поражение почечной ве&ны выявлено у 55, НПВ ниже уровня диафрагмы — у 40, на уровне диафрагмы и выше (устье НПВ) — у 9. В 10 случаях в качестве симптома тромботического процесса в почечной вене отмечено варикоцеле. От&казали в хирургическом лечении 24 больным из 104 в связи с распространенностью процесса.
Оперативное вмешательство провели 80 паци&ентам с тромботическим поражением вен. Выпол&нение стандартной нефрэктомии оказалось доста&точным для 35 больных с тромбом почечной вены, не достигавшим устья. В 24 случаях при распростра&нении тромба в НПВ с плотной фиксацией к стенке вены произведена резекция фрагмента стенки НПВ с тромбэктомией, при этом в 7 случаях для ушива&ния образовавшегося дефекта применена заплата из политетрафторэтилена. Произвели два протезиро&вания НПВ. У 19 больных при отсутствии плотной фиксации тромба к стенке НПВ и в области устья почечной вены выполнили только резекцию устья почечной вены с ушиванием дефекта НПВ в попе&речном или продольном направлении. Тромбэкто-мию проводили в условиях гепаринизации после пережатия НПВ выше и ниже тромба, контралате-ральной почечной вены, крупных поясничных вен. В ряде случаев, после мобилизации НПВ, оказыва&лось возможным сместить пальцами верхушку тром&ба дистально, что позволяло накладывать зажим на более низком уровне.
При распространении тромба в ретропеченоч-ный сегмент и выше мобилизовали печень с ее со&судистой изоляцией (включая пережатие гепатодуо-денальной связки). Если тромбоз достигал входа в предсердие, проводили диафрагмотомию, что по&зволяло наложить зажим проксимальнее верхушки тромба.
В одном случае НПВ лигировали во время опе&рации по причине распространения тромбоза до подвздошных вен и отсутствия адекватного притока крови по ним.
Методов вспомогательного и искусственного кровообращения, временного шунтирования мы не применяли.
Кровопотеря во время операции составляла 300-2500 мл (в среднем 750 мл). В течение послед&него года для реинфузии крови у 8 больных исполь&зовали аппарат Fresenius HemaCare С.А.Т.8. plus.
После вмешательства на НПВ назначали внача&ле гепарин, а затем один из фракционированных ге-паринов. Вопрос о назначении непрямых антикоа&гулянтов решали индивидуально. У ряда пациентов без значимых стенозов НПВ после ушивания стенки при отсутствии имплантатов считали возможным назначение дезагрегантной терапии.
Результаты и обсуждение
Двое пациентов умерли во время операции и еще трое в последующие 3 сут после операции. В 1 случае к летальному исходу привела массивная ТЭЛА, развившаяся интраоперационно, в осталь&ных — кровопотеря с последующим развитием ДВС-синдрома. У 2 пациентов в отдаленном периоде об&наружили тромботическую окклюзию НПВ, при этом в одном наблюдении она протекала бессимп&томно. В остальных случаях установлена проходи&мость полой вены после реконструктивного вмеша&тельства (рис. 2). Летальность составила 6,25% при годичной выживаемости 90% и пятилетней 54,1%.
Хирургическое лечение остается основным ме&тодом лечения почечно-клеточного рака, при этом тромбоз НПВ на сегодняшний день не может слу&жить основанием для отказа от оперативного лече&ния. Даже при отдаленных метастазах успешная нефрэктомия с тромбэктомией улучшают прогноз[9, 10]
Общепринятой классификации тромбоза по уровню распространения не существует. Предло&женное в 1987 г. R. Neves [11] разделение (в модифи&кации Nesbitt J.) выглядит следующим образом:
уровень I — подпеченочный;
уровень II — внутрипеченочный;
уровень III — надпеченочный;
уровень IV — с распространением в предсердие.
Контрастируется полая вена, дефект которой был ушит с приме&нением заплаты из политетрафторэтилена.
С учетом необходимости применения разных тактических подходов G. Ciancio [12] предложил разделить III уровень на подгруппы:
Ша — тромб ниже главных печеночных вен;
IIIb — тромб на уровне главных печеночных вен с возможным проникновением в них;
Шс — тромб выше устьев главных печеночных вен, но ниже диафрагмы;
IIId — тромбоз с распространением в интрапе-рикардиальный отдел НПВ, но не в предсердие.
Более простой вариант предложен D. Skinner в 1989 г. и S. Babu в 1998 г. [13, 14]:
уровень I — подпеченочный;
уровень II — ретропеченочный — грудной;
уровень III — с распространением в предсердие.
Выживаемость и процент осложнений колеб&лются в достаточно большом диапазоне, что легко объяснимо разнородностью групп пациентов. В се&рии из 55 больных (T. Terakawa), оперированных в университетской клинике г. Кобэ в период с 1983 по 2005 г., трех- и пятилетняя выживаемость составила 51,4 и 30,3% соответственно при послеоперацион&ной смертности 3,6% [6].
Тромботические осложнения рака почки неред&ко бессимптомны. Из 122 пациентов, последова&тельно оперированных M. Galucci по поводу почеч-но-клеточного рака, тромбоз НПВ был отмечен у 15 (12,3%). Симптомы в виде отеков нижних конечно&стей наблюдались у 5 пациентов, одышка с болями в грудной клетке — у 1. В 4 случаях тромботические симптомы были единственным проявлением опухо&ли. В 10 случаях тромб находился в позадипеченоч-ном сегменте НПВ и достигал предсердия в 1 случае.
Среднее время операции в настоящем исследовании составило 256 мин, кровопотеря — 450 мл. При среднем сроке наблюдения 54 мес один пациент умер от генерализации опухолевого заболевания, все остальные были живы без признаков тромбоза или рецидива. М. Galucci во всех случаях применял только лапаротомный доступ, при высоком тромбо&зе дополняя его полной мобилизацией печени с ее медиальной ротацией [15].
Если при подпеченочном тромбозе вопросы до&ступа обсуждаются нечасто (практически всегда — лапаротомия), то при распространении тромба до предсердия предлагаются различные варианты. Воз&можна лапароторако(стерно)томия с вспомогатель&ным кровообращением, искусственным кровообра&щением или циркуляторным арестом. Несмотря на эффективность с онкологической точки зрения, удаление распространяющихся до предсердия тром&бов сопровождается большим процентом осложне&ний и смертности. Торакофренолапаротомия при удалении опухолевого тромба у 53 пациентов, по данным D. Skinner, сопровождалась смертностью 13,2% со средней кровопотерей 5446 мл [16]. О при&менении методики полной изоляции ретропеченоч-ного сегмента НПВ из лапаротомного доступа за счет выделения печени и ее медиальной ротации с целью тромбэктомии впервые сообщил трансплан&толог из Университета Майами G. Ciancio в 2000 г. Им были оперированы 7 пациентов с ретропеченоч-ным тромбозом [12]. Альтернативный вариант до&ступа к НПВ, предусматривающий сегментэктомию хвостатой доли печени, был предложен S. Ohwada [17].
Как показывает наш собственный опыт и на&блюдения других авторов, наибольшими затрудне&ниями сопровождаются манипуляции на ретропече-ночном сегменте НПВ. Стенка сосуда на этом уров&не хрупкая и может быть окружена тканью печени. Печеночные вены короткие, добавочные печеноч&ные вены разнообразны как по расположению, так и по количеству. В условиях окклюзии НПВ гипер&трофированное коллатеральное русло в виде тонко&стенных, хаотично расположенных вен дополни&тельно усложняет ситуацию. Для полного удаления тромба без риска фрагментации и эмболии необхо&дим уверенный контроль над всеми крупными сосу&дами в зоне вмешательства. Нельзя оставлять без внимания поясничные вены, кровотечение из кото&рых может быть весьма интенсивным. Попытки «слепого» удаления тромба (например, баллонным зондом) несут дополнительную опасность оставле&ния на стенке вены резидуальных тромботических масс, которые могут содержать опухолевые клетки. Это значительно увеличивает не только риск ТЭЛА в послеоперационном периоде, но также вероят&ность генерализации опухолевого процесса и мест&ного рецидива.
1. Тромбоз почечных вен и НПВ в большинстве случаев можно обнаружить только на основании ре&зультатов инструментальных методов исследования, поскольку клинические проявления данного ослож&нения рака почки скудны или вообще отсутствуют.
2. Ультразвуковое исследование пациентов при раке почки должно включать осмотр почечной вены с допплеровским исследованием. При обнаружении тромбоза обязательно осматривают НПВ.
3. Каваграфию нужно выполнять во всех случаях при подозрении на тромб в НПВ, при этом обяза&тельна визуализация печеночных вен.
4. Нефрэктомия с тромбэктомией из НПВ со&провождается приемлемыми показателями леталь&ности и осложнений.
А.А. ФОКИН, П.А. КАРНАУХ, О.С. ТЕРЕШИН
Уральская государственная медицинская академия дополнительного образования Росздрава, Челябинский областной клинический онкологический диспансер, Челябинск
ФЛЕБОЛОГИЯ, 3, 2008
ЛИТЕРАТУРА
1. Щукин Д.В., Илюхин Ю.А. Хирургия опухолевых тромбов нижней по&лой вены при раке почки. Белгород 2007; 196.
2. Marshall F.F., Dietrich D.D., Baumgartner W.A., Reitz B.A. Surgical management of renal cell carcinoma with intracaval neoplastic extension above the hepatic veins. J Urol 1988; 139: 1166-1172.
3. Blute M.L., Leibovich B.C., Lohse C.M. et al. The Mayo Clinic experience with surgical management, complications and outcome for patients with renal cell carcinoma and venous tumour thrombus. BJU Int 2004; 94: 33-41.
4. Parekh D.J., Cookson M.S., Chapman W. et al. Renal cell carcinoma with renal vein and inferior vena caval involvement: Clinicopathological fea&tures, surgical techniques and outcomes. J Urol 2005; 173: 1897-1902.
5. Kim H.L., Zisman A., Han K.R. et al. Prognostic significance of venous thrombus in renal cell carcinoma. Are renal vein and inferior vena cava in&volvement different? J Urol 2004; 171: 588-591.
6. Terakawa T., Miyake H., Takenaka A. et al. Clinical outcome of surgical management for patients with renal cell carcinoma involving the inferior vena cava. Int J Urol 2007; 14: 9: 781-784.
7. Давыдов М.И. Эволюция онкохирургии и ее перспективы. Материалы III съезда онкологов и радиологов СНГ. Минск: ОДО Тонпик 2004; 36-42.
8. Переверзев А.С. Хирургия опухолей почки и верхних мочевых путей. Харьков 1997; 394.
9. Slaton J.W., Balbay M.D., Levy D.A. et al. Nephrectomy and vena cava thrombectomy in patient with metastatic renal cell carcinoma. Urology 1997; 50: 673-677.
10. Nesbitt J.C., Soltero E.R., Dinney C.P. et al. Surgical treatment of renal cell carcinoma with inferior vena cava tumor thrombus. Ann Thorac Surg 1997; 63: 1592-1600.
11. Neves R.J., Zincke H. Surgical treatment of renal cancer with vena cava extension. Br J Urol 1987; 59: 390-395.
12. Ciancio G., Hawke C., Soloway M. The use of liver transplant techniques to aid in the surgical management of urological tumors. J Urol 2000; 164 (3 Pt 1): 665-672.
13. Skinner D.G., Pritchett T.R., Lieskovsky G. et al. Vena cava involvement by renal cell carcinoma. Surgical resection provides meaningful long term sur&vival. Ann Surg 1989; 210: 387-392.
14. Babu S.C., Mianoni T., Shah P.M. et al. Malignant renal tumor with exten&sion to the inferior vena cava. Am J Surg 1998; 176: 137-139.
15. Galucci M., Borzomati D., Flammia G. Liver harvesting technique for the treatment of retro-hepatic caval thrombosis concomitant to renal-cell carci&noma: perioperative and long-term results in 15 patients without mortality. Eur Urol 2004; 45: 194-202.
16. Skinner D.G., Pfister R.F., Colvin R. Extension of renal cell carcinoma into the vena cava: the rationale for aggressive surgical treatment. J Urol 1972; 107: 711-716.
17. Ohwada S., Satoh Y., Tanahasi Y. et al. Left-sided approach to renal cell carcinoma tumor thrombus extending into suprahepatic inferior vena cava by resection of the left caudate lobe. Angiology 1997; 48: 7: 629-635.
Рак почки с массивным тромбозом нижней полой вены. Хирургическое лечение Текст научной статьи по специальности «Медицина и здравоохранение»
Аннотация научной статьи по медицине и здравоохранению, автор научной работы — Хвастунов Р.А., Юсифова А.А.
Представлены клинические примеры хирургического лечения рака почки с экстремально высокими тромбами
Похожие темы научных работ по медицине и здравоохранению , автор научной работы — Хвастунов Р.А., Юсифова А.А.,
RENAL CANCER ACCOMAPNIED BY SEVERE THROMBOSIS OF THE INFERIOR VENA CAVA: A SURGICAL APPROACH
The article presents a series of case reports of surgical treatment of renal cancer accompanied by severe thrombosis of the inferior vena cava .
Текст научной работы на тему «Рак почки с массивным тромбозом нижней полой вены. Хирургическое лечение»
В ПОМОЩЬ ПРАКТИЧЕСКОМУ ВРАЧУ
РАК ПОЧКИ С МАССИВНЫМ ТРОМБОЗОМ НИЖНЕЙ ПОЛОЙ ВЕНЫ.
Р. А. Хвастунов, А. А. Юсифова
Волгоградский государственный медицинский университет, кафедра онкологии с курсом онкологии и гематологии ФУВ, Волгоградский областной клинический онкологический диспансер
Представлены клинические примеры хирургического лечения рака почки с экстремально высокими тромбами. Ключевые слова: рак почки, тромбоз нижней полой вены.
RENAL CANCER ACCOMAPNIED BY SEVERE THROMBOSIS OF THE INFERIOR VENA CAVA: A SURGICAL APPROACH
R. А. Khvastunov, A. A. Yusifova
Volgograd State Medical University, Department of Oncology with the Course of Oncology and Haematology,
Department of Continuing Education, Volgograd Regional Oncology Dispensary
The article presents a series of case reports of surgical treatment of renal cancer accompanied by severe thrombosis of the inferior vena cava.
Key words: renal cancer, thrombosis of the inferior vena cava.
Опухоли почки стали описывать в литературе около 150 лет назад. Одним из первых в 1826 г. о них сообщил Konig, который описал двух больных с «медуллярной саркомой» почки, потом в 1883 г. — Grawitz, после чего эти опухоли стали называть по его имени. В 1921 г. опухоли почки получили название «гипернефрома», а затем — «гипернефроидный рак». В 1964 г. Riches дал подробное описание опухоли Гравитца, или гипернефромы, и показал, что это не что иное, как аденокарцинома,
которая происходит из эпителия различных отделов не-фрона и собирательных трубочек и составляет около 3 % всех новообразований и 90 % всех видов опухолей почки. В настоящее время эти опухоли называют «рак почки», а морфологически описывают как почечно-кле-точный рак [1 ], атрибутом которого является способность к традиционной инвазии в окружающие ткани. Зависимость выживаемости пациентов от глубины периреналь-ного прорастания представлена на рис. 1.
Стадия I Опухоль 7см, не выходит за пределы почки; пятилетняя выживаемость 88%
СтаДИЯ III Рек поражает крупные сосуды, надпочечники. 1 регионарный лимфоузел, не выходит за пределы фасции Герота; пятилетняя выживаемость 5996
Стадия IV Опухоль распространяется за пределы фасции Герота, поражает более 1 регионарного узла Пятилетняя выживаемость 20%
Нижняя полая вена
Рис. 1. Пятилетняя выживаемость при раке почки в зависимости от стадии ^^^^^^^^ Выпуск 2 (62). 2017 =
Отличительной особенностью рака почки (РП) является частое, по сравнению с другими опухолями, его распространение по венозным коллекторам как по пути наименьшего сопротивления инвазивному росту, а именно по почечной и нижней полой вене (НПВ) вплоть до правого предсердия. Термин венозная инвазия означает проникновение опухоли в просвет сосудов (продолженный рост) без обязательного прорастания сосудистой стенки. Протяженность таких тромбов может достигать 20 см. Они фиксированы к опухоли в паренхиме почки и флотируют на разном уровне в просвете НПВ. Предложенная в 1987 г R. Neves [1] классификация тромбов НПВ (в модификации Nesbitt J.) выглядит следующим образом:
уровень I — подпеченочный; уровень II — внутрипеченочный; уровень III — надпеченочный; уровень IV—с распространением в предсердие. Весьма оригинальный подход с систематизацией опухолевых венозных тромбов предложен Bachmann [1]. При этом в качестве определяющего параметра используется разделение тромбов на требующие остановки сердца и использования аппарата искусственного кровообращения и не требующие:
1 тип. Не требующие остановки системного кровообращения малые интракавальные тромбы; четко выявленная подпеченочная локализация края тромба.
2 тип. Оборудование для остановки системного кровообращения должно быть подготовлено, но может не понадобиться.
2а тип. Остановка кровообращения, возможно, потребуется, в операционной имеется оборудование для вено-венозного шунтирования: супрагепатические, но инфрадиафрагмальные тромбы; супрадиафрагмаль-ные свободно флотирующие тромбы.
2в тип. Необходимость в остановке кровообращения четко определена: опухоль инфильтрирует сосудистую стенку в супрагепатическом отделе НПВ в области печеночных вен или правого предсердия; большие супрагепатические тромбы; тромбы, при которых высоко вероятна эмболия.
Классификация опухолевых тромбов согласно клинике Мейо (рис. 2):
Рис. 2. Уровни поражения нижней полой вены опухолевым тромбом
0. Тромб ограничен почечной веной.
1. Тромб НПВ менее чем на 2 см выше почечной
II. Тромб более чем на 2 см выше почечной вены, но ниже печеночных вен.
III. Тромб на уровне или выше печеночных вен, но ниже диафрагмы.
IV. Тромб выше диафрагмы.
В зависимости от протяженности и отношения к печеночным венам выделяют 4 вида тромбов НПВ (Novick): периренальные, субпеченочные, внутрипеченоч-ные (ретропеченочные) и надпеченочные. Первые три вида относят к группе поддиафрагмальных тромбов. Надпеченочные, они же наддиафрагмальные тромбы, подразделяют на внутриперикардиальные и внутрипред-сердные. Уровень распространения тромба является важным фактором при выборе метода хирургического лечения. Для планирования техники операции и прогнозирования результатов лечения большое значение имеет не только протяженность опухолевого тромба, но и степень его фиксации и врастания в сосудистую стенку.
Хирургия опухолевых тромбов нижней полой вены представляет собой одну из самых сложных проблем он-коурологии. Считается, что проникновение почечно-кле-точного рака в просвет почечной вены имеет место в 25— 30 % наблюдений, а распространение в нижнюю полую вену — в 4—10 % случаев [1]. Хирургическое лечение остается основным методом лечения почечно-клеточно-го рака, при этом тромбоз НПВ на сегодняшний день не может служить основанием для отказа от оперативного лечения. Даже при отдаленных метастазах успешная не-фрэктомия с тромбэктомией улучшают прогноз. Основным отличием тромбэктомии от просто радикальной не-фрэктомии является необходимость мобилизации, контроля и резекции НПВ, что превращает обычную полостную операцию в сосудистую и может представлять определенные технические сложности. Удаление тромба при его распространении на правое предсердие особенно опасно и при некоторых видах тромбоза, требующего кардио-пульмонального шунтирования, гипотермии с остановкой кровообращения. [2] Применение кардиопульмонально-го шунтирования показано для удаления фиксированных тромбов, распространяющихся выше диафрагмы, когда использование более простых методов опасно в отношении фрагментации опухоли и развития тромбоэмболичес-ких осложнений. Обычно, даже если опухолевый тромб не распространяется в предсердие, необходим аппарат искусственного кровообращения, который подключает к бедренным сосудам бригада кардиохирургов.
За последние 5 лет мы наблюдали 15 больных с РП, осложненным сосудистым тромбозом. У 12 из них тромбы располагались в почечной вене либо имели минимальное распространение в НПВ. Операции в этих случаях мало отличались от традиционных нефрэктомий (НЭ). Верхушку опухолевого тромба в 6 случаях мы дистально низводили в ренальную вену, которую после этого типично лигировали и пересекали. Еще в 6 случаях требова-
лась краевая резекция НПВ, отжатой зажимом Сатинско-го вокруг устья пораженной почечной вены с последующим сосудистым швом. Дважды мы оперировали больных с опухолевыми тромбами на уровне печеночных вен, когда выделяли НПВ до диафрагмы, лигировали печеночные и поясничные вены, проводили сосудистую изоляцию НПВ и использовали CellSaver. Еще один раз мы оперировали пациента с экстремально высоким опухолевым тромбом, распространяющимся выше уровня диафрагмы. Описание двух случаев мы приводим подробно.
Случай 1. Пациентка Ч., 69 лет, консультирована нами в январе 2017 года в поликлинике ВОКОД без существенных жалоб по представлению химиотерапевта. В анамнезе — острый инфаркт миокарда в 2013 году, паллиативная НЭ слева в 2015 году с последующей иммунотерапией интерфероном-альфа-2-Ь по 6 000 000 МЕ 3 раза в неделю в течение 6 месяцев. По данным серийных трансабдоминальных УЗИ ОБП констатирован тромб НПВ протяженностью 8 см, стабильный в течение 1,5 лет наблюдения. Из протокола операции, выполненной 17.05.2015г. в урологическом отделении ВОКОД, следует, что в объеме НЭ слева удалены опухоль диаметром 10 см (светлоклеточная аденокарци-нома) с лигированием левой почечной ножки и оставлением тромба размерами 6х8 см в НПВ.
Мы обратили внимание, что в течение 1,5 лет наблюдения тромб НПВ не прогрессировал, метастазы отсутствовали, и сочли, что возможности хирургического метода лечения у этой больной не исчерпаны. 20.01.2017 г. в условиях клиники № 1 ВолгГМУ мы предприняли диагностические ангиохирургические интервенции. При коронарокардиографии сердечные ресурсы признаны удовлетворительными, на венокаваграфии (рис. 3) визуализирован тромб НПВ, размерами 8х6 см, предположительно фиксированный в культе левой ре-нальной вены, подвздошно-бедренный венозный сегмент проходим с обеих сторон.
Рис. 3. Венокаваграфия с тромбом НПВ (маркирован стрелкой)
КТ ОБП от 29.12.2016 г.: тромб в нижней полой вене 5,6х5,1х8,0 см; с признаками сохраняющегося кровотока. Отдаленных метастазов нет (рис. 4).
Рис. 4. Опухолевый тромб в нижней полой вене на уровне интеграции с правой почечной веной.
Единственная правая почка.
Диагноз: ЗНО левой почки T3bN0M0. Тромб НПВ.
Состояние после паллиативной НЭ
26.01.2017 г. нами выполнена верхне-срединная лапаротомия. При ревизии — весь супраренальный отдел НПВ вплоть до диафрагмы представлен тромбом, расширяющим диаметр вены до 8 см. Вена выделена на всем ее протяжении с перевязкой 9 ее притоков из печени. Поясничные вены не выражены. Пережатие вены на лигатурах в инфраренальном, правом почечном и поддиафрагмальном сегменте (рис. 5). Венока-ватомия с резекцией культи левых ренальных сосудов (рис. 6) и тромбэкстракцией с поддержкой CellSaver. Суммарная кровопотеря составила 1,4 л, реинфузия отмытых эритроцитов в объеме 300 мл, инфузия заранее приготовленной аутоплазмы (1 литр) и аутокрови (450 мл). Дефект НПВ протяженностью 10 см ушит непрерывным швом нитью
Свидетельство о регистрации СМИ Эл № ФС77-52970
Источники: http://www.urolog-site.ru/oper/oper/invaz-rak-pochki.html, http://oncogram.ru/view_page.php?page=204, http://cyberleninka.ru/article/n/rak-pochki-s-massivnym-trombozom-nizhney-poloy-veny-hirurgicheskoe-lechenie