Венозный тромбоз патологическая физиология
Патологическая физиология
Общая патофизиология
Частная патофизиология
Вход в систему
Поделиться
Тромбоз — это прижизненный процесс образования в просвете кровеносного сосуда плотных масс, состоящих из элементов крови и в той или иной степени препятствующих движению крови по сосудам.
Анализируя данное определение, необходимо обратить внимание на два следующих момента. Во-первых, тромбоз является прижизненным явлением, отличаясь тем самым от посмертного свертывания крови. Тромб фиксирован на сосудистой стенке, а посмертный сгусток крови лежит в просвете сосуда свободно и легко может быть из него удален. Это обстоятельство имеет важное значение в судебно-медицинской практике, когда необходимо установить причину смерти и время ее наступления. Во-вторых, тромбоз — это не только свертывание крови, а сложный процесс, который включает в себя ряд стадий и ведет к образованию в просвете сосуда плотных масс, состоящих из кровяных элементов. Свертывание крови — это только один из компонентов тромбоза.
Причиной образования тромба является нарушение целостности стенки сосуда. В результате такого повреждения начинают функционировать следующие механизмы:
1. В нормальном кровеносном сосуде с неповрежденной стенкой наблюдается ламинарный кровоток, когда слои крови скользят друг относительно друга линейно. При нарушении целостности стенки сосуда в месте этого повреждения ламинарный кровоток сменяется турбулентным, то есть возникают завихрения жидкости, что способствует задержке форменных элементов крови около сосудистой стенки и создает основу для формирования тромба.
2. При повреждении сосудистой стенки этот ее участок становится смачиваемым, то есть капли жидкости начинают прилипать к стенке сосуда. Это тоже способствует фиксации на ней форменных элементов крови.
3. В норме форменные элементы крови и сосудистая стенка имеют одинаковый электрический заряд, что приводит к их взаимному отталкиванию. В месте повреждения сосудистая стенка заряд теряет, благодаря чему форменные элементы крови оседают на этом месте.
4. При повреждении стенки сосуда из нее в кровь выделяется тканевой тромбопластин который, вступая в реакцию с другими факторами свертывания, дает толчок коагуляции крови, что также необходимо для образования тромба.
Тромбообразованию способствуют два фактора:
1. Замедчение кровотока. Чем быстрее кровоток в сосуде, тем труднее форменным элементам удерживаться около сосудистой стенки, даже несмотря на ее повреждение. Например, при выраженном атеросклерозе наиболее сильно повреждается стенка восходящей аорты. Однако в этой части аорты тромбы образуются очень редко, так как скорость кровотока здесь столь велика, что начинающий формироваться тромб все время отрывается от стенки и уносится током крови. Наиболее же часто тромбы образуются в венах, где кровоток резко замедлен. Поэтому любой фактор, вызывающий замедление кровотока в сосудах, будет способствовать тромбообразованию.
2. Изменения физико-химических свойств крови, приводящие к повышению ее свертываемости. Например, при таком заболевании, как эритремия, при котором значительно увеличивается количество всех форменных элементов крови, в том числе и кровяных пластинок — тромбоцитов, и возрастает вязкость крови, очень часто возникает генерализованный тромбоз сосудов, от чего больной и погибает.
Однако оба указанных фактора остаются лишь условиями, способствующими тромбообразованию, но не более. Если нет повреждения сосудистой стенки, тромб не образуется, даже если в сосуде замедлился кровоток и изменились физико-химические свойства крови. И только повреждение стенки сосуда является инициирующим моментом тромбообразования.
Различают три вида тромбов:
1. Белый (агглютинационный) тромб. В его образовании главную роль играют процессы агглютинации (склеивания) форменных элементов крови — главным образом тромбоцитов и лейкоцитов. Этот тромб имеет белый цвет.
2. Красный (коагуляционный) тромб. В его образовании главную роль играют процессы коагуляции (свертывания) крови. В петлях фибрина при образовании этого тромба в большом количестве задерживаются эритроциты, поэтому данный тромб имеет красный цвет.
Поскольку процесс коагуляции протекает быстрее, чем процесс агглютинации, красный тромб образуется скорее, чем белый. Поэтому в аварийных ситуациях, когда требуется быстрое формирование тромба (например, при кровотечении), образуются преимущественно красные тромбы.
3. Смешанный тромб. Он встречается наиболее часто. В образовании этого вида тромба попеременно принимают участие процессы и агглютинации, и коагуляции. На разрезе такой тромб имеет слоистый характер. Головка смешанного тромба, то есть его часть, прикрепляющаяся к сосудистой стенке, как правило, бывает белой, тело — слоистым, а хвост — красным.
В процессе тромбообразования различают три стадии:
Первая стадия заключается в прилипании тромбоцитов к волокнам коллагена, которые выступают в просвет сосуда после повреждения его эндотелия. Тромбоциты могут прилипать и непосредственно к поврежденному эндотелию.
На второй стадии кровяные пластинки скапливаются у места повреждения стенки сосуда. При лечебном воздействии на первых двух стадиях процесс тромбообразования может оказаться обратимым.
Третья стадия характеризуется включением коагуляционных механизмов. В результате образуется фибрин, который, как сетью, опутывает тромбоциты, лейкоциты и эритроциты. Затем происходит ретракция (сжатие) кровяного сгустка и формирование тромба завершается. Третья стадия представляет собой комплекс химических реакций, идущих только слева направо, то есть данная стадия в химическом (а следовательно, и в биологическом) отношении является необратимой.
Степень нарушения функции органов при тромбозе зависит от его исхода, который может быть следующим:
1. Организация тромба, то есть его прорастание соединительной тканью. В этом случае он прочно закрепляется в сосуде и в зависимости от величины тромба и диаметра просвета сосуда, в котором он образовался, тромб в той или иной степени нарушает движение крови по сосудам.
2. Отрыв тромба и его превращение в эмбол. В этом случае оторвавшийся тромб переносится током крови в другие регионы тела закупоривает сосуд, через который он не может пройти, и вызывает нарушения местного кровообращения в данной области.
3. Канализация тромба. Если тромб рыхлый, а напор крови в сосуде высок, то кровь может проделать в сосуде канал, и кровоток, таким образом, полностью или частично (это зависит от диаметра канала) восстановится.
4. Гнойное расплавление тромба. При инфицировании тромба в области, где он расположен, может начаться гнойное воспаление. От тромба станут отрываться кусочки и превращаться в эмболы. Помимо нарушений гемодинамики, которые эти эмболы вызовут, закупоривая мелкие сосуды, они будут способствовать диссеминации микроорганизмов в различные органы и ткани.
5. Рассасывание тромба, приводящее к восстановлению кровотока в сосуде. В этом случае степень нарушения функции тканей будет зависеть от длительности процесса ишемии до момента полного рассасывания тромба.
Оценку значения тромбоза для организма следует проводить с двух позиций. Прежде всего, тромбоз — это физиологический процесс, направленный на остановку кровотечения из поврежденного сосуда. Однако при патологическом изменении стенок сосудов тромбоз из защитно-приспособительной реакции превращается в патологическую, ведет к развитию нередко очень тяжелых расстройств местного кровообращения, которые могут закончиться инвалидизацией или даже смертью больного.
35. Понятие о тромбозе. Патогенез тромбообразования. Последствие тромбозов: физиологическое и патофизиологическое значение. Тромбоэмболии.
Тромбоз- процесс прижизненного образования на внутренней поверхности стенки сосудов или в их просвете сгустков , состоящих из элементов крови и препятствующих движению крови по сосудам.
Патогенез. В механизмах развития тромбов большое участие принимают следующие патогенетические факторы(триада Вирхова). 1) повреждение сосудистой стенки (нарушение ее физико-химических свойств, питания, меаболизма). Поврежденная сосудистая стенка становится смачиваемой , теряет электрический заряд и выделяет в кровь активный тромбопластин . В результате этого элементы крови прилипают к ней. 2) повышение активности свертывающей или снижение активности противосвертывающей и фибринолитической систем крови. 3) замедление тока крови и его нарушение в виде завихрений( в области тромба , агрегатов эритроцитов, атероматозных бляшек, аневризмы сосуда). В процессе гемостаза выделяют 2 фазы: первая фаза- сосудисто-тромбоцитрная (клеточная); вторая фаза-коагуляционная(плазменная). Исходы: рассасывание тромба(с восстановлением местного кровообращения); расплавление асептическое или гнойное( с образованием абсцесса);организация( прорастание соединительной тканью, в результате чего тромб плотно фиксируется к стенке сосуда); реканализация(прорастание сосудами), особенно рыхлого тромба; отрыв тромба с образованием эмбола. Под тромбоэмболией подразумевают закупорку кровеносного сосуда тромбом — сгустком крови. Это процесс протекает остро, развивается внезапно и, нередко, становится причиной инвалидности или смерти, особенно когда закупорка локализуется в жизненно-важных органах — головном и спинном мозге, сердце, конечностей.
Тромбоэмболия не является самостоятельным заболеванием, это лишь следствие различных патологических процессов, в результате которых в сосудах образуются тромбы. Причины.
Причина тромбоэмболии — оторвавшийся тромб. Он, словно пробка, перекрывает просвет сосудов, в этом месте развивается ишемия — обескровливание.
36. Понятие об ишемии, определение. Виды, внешние признаки, механизм возникновения. Стаз, виды. Инфаркт. Под ишемией понимают умньшение кровенаполнения ткания или органа и количества протекающей через них крови, вызванные затруднением её притока по артериальным сосудам (в основном по артериолам).
Ишемия бывает двух видов : физиологическая и патологическая. Физиологическая ишемия бывает времнной , обратимой, имеет приспособительное значение , соответствует метаболическим и функциональным отребностям органа , ткани. Патологическая ишемия бывает биологически нецелесообразной , не соответствует метаболическим и функциональным потребностям органа, ткани. Ишемия характеризуется рядом следующих признаков: побледнение участка, выраженность которого зависит от степени уменьшения притока крови к нему (у животных это можно наблюдать на видимых слизистых оболочках); понижение температуры ишемизированного участка при снижении уровня обмена веществ и окислительных процессов; уменьшение его объема в результате уменьшения или прекращения притока крови и образования тканевой жидкости, при этом понижается также тургор ткани. При ишемии ухудшаются функция органа, степень чувствительности (гипостезия) из-за нарушения питания нервных окончаний (начального звена рефлекторной дуги).
В развитии ишемии выделяют несколько механизмов. Возможно возникновение ишемии в результате механического препятствия току крови — компрессионная или обтурационная ишемия. Подобные ситуации в клинической практике — нередкое явление; к ним можно отнести синдром блокады сонной артерии при ее атеросклерозе или аномалиях развития, височный гранулематозный артериит, абдоминальный ишемический синдром при атеросклерозе брыжеечных артерий, сдавление подключичной артерии гипертрофированной передней лестничной мышцей или рудиментом шейного ребра и др.
Гемодинамические механизмы имеют важное значение в развитии регионарной и органной ишемии. Так, при синдроме подключичного обкрадывания в результате блокады подключичной артерии (стеноз, атеросклероз и др.) кровь из позвоночной артерии переходит в подключичную, уменьшая кровоснабжение мозга. При синдроме брахиоцефального обкрадывания в случае блокады этого ствола кровь оттекает от мозга в сонную и подключичную артерии.
Негативный систолический эффект проявляется в миокарде, где склерозированные коронарные сосуды полностью перекрываются во время систолы. Негативный диастолический эффект связан с тем, что во время диастолы пораженные атеросклерозом артерии не раскрываются и формируется ишемия. Феномен no reflow определяется невозобновлением кровотока вследствие отека эндотелиальных клеток при ишемии. Одним из важных механизмов ишемии является нейрогенный спазм артерий мышечного типа; этот эффект может быть рефлекторной или центрогенной природы и связан с увеличением а-адренергических или холинергических влияний. В развитии ишемических состояний иногда важное значение приобретает гуморальный механизм, включающийся в результате усиленного высвобождения в кровь прессорных агентов, например ангиотензина-И, вазопрессина, катехоламинов и др.
Помимо гуморального, выделяют сенситивный механизм; он действует в случае повышения чувствительности соответствующих рецепторов миоцитов и их сокращения при нормальной концентрации прессорных агентов в крови. Факторами, повышающими чувствительность сосудов к прессорным агентам, могут быть хлорид натрия, минералокортикоиды, атеросклеротическое поражение сосуда и др. Резкое увеличение потребности органа в кислороде нередко выступает в качестве своеобразного механизма ишемии (мозг, сердце, почки), если оно сопровождается возрастанием симпатико-адреналовых влияний, анемией, дыхательной недостаточностью и др.
Стаз-прижизненнаяостановка тока крови в кровеносных и лимфатических сосудах микроциркуляторного русла. Различают ишемический , венозный, капиллярный(истинный) стаз. В основе ишемического стаза лежит резко уменьшенное или полное закрытие просвета артериального сосуда , венозного(застойного) стаза-значительное нарушение(затруднение или прекращение0 оттока крови по венам , капиллярного(истинного) стаза- первичное нарушение кровотока в капиллярах.
Инфа́ркт миока́рда — одна из клинических форм ишемической болезни сердца, протекающая с развитием ишемического некроза участка миокарда, обусловленного абсолютной или относительной недостаточностью его кровоснабжения. Другое название — сердечный приступ. Различают И. белый, или ишемический, представляющий собой зону некроза, лишённую крови, и красный, геморрагический, когда зона некроза пропитана излившейся кровью; встречается также ишемический И. с геморрагическим поясом. Первый и третий виды И. чаще образуются в сердце, почках, селезёнке, второй — в лёгких, кишечнике. И. может иметь конусовидную (почка, лёгкие) или неправильную (сердце, мозг) форму. Консистенция И. обусловлена характером некроза, который может быть сухим (инфаркт миокарда) или влажным (И. мозга). При И. возникают глубокие изменения органа: омертвевшие массы рассасываются или организуются, в результате чего образуется киста (например, в головном мозге) или рубец (например, в мышце сердца), они могут нагнаиваться и подвергаться гнойному расплавлению (септический И.). В зависимости от размеров, локализации и свойств И. происходит ослабление или выпадение функций органа.
37. Воспаление: определение, причины, основные признаки и патогенез их развития. Аутохтомность воспалительного процесса. Связь воспаления с аллергией и другими типовыми патологическими процессами. Воспале́ние (лат. inflammatio) — это комплексный, местный и общий патологический процесс, возникающий в ответ на повреждение (alteratio) клеточных структур организма или действие патогенного раздражителя и проявляющийся в реакциях (exudatio и др.), направленных на устранение продуктов повреждения, а если возможно, то и агентов (раздражителей), а также приводящий к максимальному для данных условий восстановлению (proliferatio и др.) в зоне повреждения.Воспаление – сложный типовой патологический процесс который: выработан в процессе эволюции, генетически запрограммирован, имеет преимущетвенно защитно-адаптивное значение, возникает в ответ на действие различных повреждающих фаторов, характеризуется динамическими измеениями альтерации. Для воспаления характерны пять внешних местных проявлений, которые очень наглядно выступают при ожоге кожи: 1) краснота (rubor), 2) припухлость (tumor), 3) повышение температуры (calor), 4) боль (dolor), 5) нарушение функций органа (functio laesa).
При раздражении кожи или слизистых оболочек рефлекторно происходит расширение капилляров и в данном месте наблюдается прилив крови, вследствие чего появляется краснота. Стенки сосудов становятся порозными, в окружающую ткань начинает пропотевать жидкая часть крови, проникают белок и форменные элементы крови, в результате чего образуется воспалительный выпот — экссудат, который и обусловливает отек — припухлость кожи. Вследствие прилива крови к воспаленному участку и повышенного обмена веществ в пораженной ткани наблюдается местное повышение температуры — даже на ощупь кожа в очаге воспаления становится более горячей по сравнению с окружающей здоровой кожей. Боль возникает вследствие раздражения чувствительных нервных окончаний болезнетворным фактором, а также в результате сдавления и раздражения последних экссудатом. Нарушение функции органа обусловлено тем, что измененная патологическим процессом ткань не может функционировать как здоровая: нарушаются осязание, потоотделение и другие функции кожи.
Причинами воспаления могут быть всевозможные экзогенные раздражения, исходящие из внешней среды.
Следовательно, причинами воспаления могут быть механические, физические, химические и биологические воздействия на весь организм или на отдельные его части и органы. Поэтому многие заболевания, вызываемые внешними факторами, сопровождаются тем или иным воспалительным процессом. Кроме того, причинами воспаления могут быть и эндогенные раздражения— вредные вещества, образующиеся в самом организме.
Механизмы определяющие начало процесса, его развитие и исход:
повреждение от действия флогогенного агента (первичная альтерация);
выброс из клеток и образование биологически активных веществ — медиаторов воспаления, освобождение и активация лизосомальных ферментов, действие их на биологические макромолекулы (вторичная альтерация);
нарушения микроциркуляции, повышение проницаемости стенки сосудов, экссудация;
размножение клеток (пролиферация);
38. Первичная и вторичная альтерация. Роль клеточных и гуморальных факторов в развитии вторичной альтерации. Термин альтерация ознчает раздражение и повреждение рецепторов, мембран, внутриклеточных органелл(особенно ядер, лизосом, митохондрий), целых клеток, межклеточного вещества , периферических(особенно терминальных) , кровеносных и лимфатических сосудов. Альтерация – это первое и непосредственное следствие действия флогогенного и патогенетических факторов. Она включает комплекс комплекс обменных , физико-химических , структурных и функциональных изменений в поврежденных и близлежащих тканях. Морфологически она проявляется различными формами и степенями дистрофии, паранекроза, некробиоза, некроза. Альтерация как правило становится пусковым звеном патогенеза развития различных патологических процессов , состояний и болезней. Различают два вида альтерации : первичную и вторичную. Первичная альтерация возникает в ответ на прямое действие воспалительного (флогогенного) фактора и пролонгирует его патогенное действие . Степень и характер альтерации зависит от интенсивности и качества флогогенного фактора , а также от локализации и площади повреждения , реактивности и резистентности поврежденных структур и организма в целом. Вторичная альтерация возникает под влиянием различных патогенетических факторов: как местных изменений (физико-химических факторов , количества и активности медиаторов воспаления, сосудистых реакций) , так и системных( нервной и гуморальной в том числе эндокринной и иммунной) реакций. Соотношение выраженности первичной и вторичной альтерации может быть различным . Это соотношение обусловлено объёмом и характером ткани , главным образом количеством вовлеченных в патологический процесс сосудов( кровеносных и лимфатических) и нервных структур. Обычно чем больше первичная альтерация , тем больше вторичная альтерация . Но при чрезмерно выраженной первичной альтерацией (глубокий некроз, обугливаниеЯ, промерзание) вторичная альтерация может быть не большей, а такой же или даже значительно меньшей степени.
Медиаторы биохимической фазы альтерации в зависимости от их происхождения принято делить на гуморальные и клеточные. В свою очередь, клеточные медиаторы подразделяются на существующие и вновь образованные на фоне воздействия альтерирующего фактора.
К гуморальным медиаторам относят кинины, активные компоненты комплемента (С5а, С3а, С3b, комплекс С5а — С9а, С5а des Arg) , а также факторы систем гемостаза и фибринолиза [46, 66]. К числу клеточных существующих медиаторов относят вазоактивные амины (гистамин, серотонин), лизосомальные ферменты, неферментные катионные белки, нейропептиды (вещество Р, кальцитонин-генсвязанный пептид, нейрокинин).
Вновь образующиеся в зоне альтерации медиаторы клеточного происхождения представлены метаболитами арахидоновой кислоты (простагландины, тромбоксаны, лейкотриены), цитокинами, ферментами, а также активными метаболитами кислорода (гидроксил, супероксид анион-радикал, пергидроксил, перекись водорода, синглетный молекулярный кислород).
Касаясь динамики освобождения медиаторов воспаления в зоне альтерации, следует отметить инициирующую роль гистамина, нейромедиаторов и липидомедиаторов. Показано, что в первые секунды после повреждения сенсорные пептидергические волокна, участвующие в ноцицепции, выделяют особые сенсорные нейропептиды: субстанцию Р, пептид гена, родственного кальцитонину, и пептид протеинового гена .
Указанные нейромедиаторы вызывают выраженную вазодилатацию, а также индуцируют экспрессию молекул межклеточной адгезии на поверхности лейкоцитов и эндотелиальных клеток, стимулируя тем самым эмиграцию лейкоцитов. Пептид гена, родственного кальцитонину, стимулирует пролиферацию эндотелиальных клеток, а субстанция Р индуцирует выработку фактора некроза опухоли (ФНО-α) в макрофагах. Кроме того, сенсорные нейропептиды стимулируют продукцию макрофагами цитокинов, влияют на иммуногенез, модулируют пролиферацию Т-лимфоцитов.
39. Причины и механизм изменения обмена веществ в очаге воспаления. Роль продуктов нарушенного обмена веществ (физико-химических изменений) в развитии воспаления. Интенсивность обмена веществ при воспалении, особенно в центре очага, повышается. Освобождающиеся из поврежденных лизосом ферменты гидролизуют находящиеся в очаге углеводы, белки, нуклеиновые кислоты, жиры. Продукты гидролиза подвергаются воздействию ферментов гликолиза, активность которых также повышается. Это относится и к ферментам аэробного окисления. Для характеристики метаболизма при воспалении издавна применяется термин «пожар обмена». Аналогия состоит не только в том, что обмен веществ в очаге воспаления резко повышен, но и в том, что «горение» происходит не до конца, а с образованием недоокисленных продуктов (полипетиды, жирные кислоты, кетоновые тела).
Следовательно, воспаление всегда начинается с усиления обмена веществ. Этим в значительной степени объясняется один из кардинальных признаков процесса — повышение температуры. В дальнейшем интенсивность метаболизма снижается, а вместе с этим изменяется и его направленность. Если сначала, т. е. в остром периоде воспаления, преобладают процессы распада, то в дальнейшем — процессы синтеза. Разграничить их во времени практически невозможно. Когда преобладают катаболические процессы, наблюдаются деполимеризация белково-гликозаминогликановых комплексов, распад белков, жиров и углеводов, появление свободных аминокислот, полипептидов, аминосахаров, уроновых кислот: Некоторые из образующихся веществ представляют особый интерес (кинины, простагландины), так как, включаясь в динамику воспаления, они придают ему определенный оттенок.
Анаболические процессы появляются очень рано, но преобладают на более поздних стадиях воспаления, когда проявляются восстановительные (репаративные) тенденции. В результате активирования определенных ферментов усиливается синтез ДНК и РНК, повышается активность гистиоцитов и фибробластов. В связи с повышением в них активности ферментов окислительно-восстановительных процессов активируются процессы окисления и окислительного фосфорилирования, увеличивается выход макроэргов.
Физико-химические изменения в очаге воспаления. Вследствие нарушения тканевого окисления и накопления в тканях недоокисленных продуктов развивается ацидоз. Сначала он компенсируется буферными механизмами, а затем становится декомпенсированным, в результате чего рН экссудата снижается. Концентрация ионов водорода тем выше, чем интенсивнее выражено воспаление. При остром абсцессе рН гноя может снизиться до 5,3. Наряду с повышенной кислотностью в воспаленной ткани повышается осмотическое давление, что является результатом усиления катаболических процессов: крупные молекулы расщепляются на более мелкие, их концентрация повышается. Увеличивается также содержание электролитов (ионов Na, К, Са). Концентрация ионов калия, освобождающегося из гибнущих клеток, в гнойном экссудате может достигать 256 — 511 ммоль/л (100 — 200 мг %), тогда как в нормальных тканях она не превышает 51,5 ммоль/л (20 мг %). Определение осмотического давления по снижению показателя точки замерзания экссудата показало, что депрессия составляет 0,6 — 0,8, что в пересчете на единицы измерения давления свидетельствует о повышении с 759 — 800 кПа (7,5 — 7,9 амт) в норме до 810 — 1114 кПа (8—11 атм) при воспалении (Шаде).
Ацидоз обусловливает набухание элементов соединительной ткани.
Повышение осмотического давления усиливает экссудацию и местный отек.
Этим объясняются главные признаки воспаления — появление припухлости и боли, наличие которой тоже в значительной степени объясняется натяжением ткани, возникающим при припухлости.
Венозный тромбоз
Этиология и патофизиология
- При поверхностном венозном тромбозе (ПВТ) в процесс вовлекаются поверхностные вены верхних или нижних конечностей (v. cephalica, v. basilica).
- При тромбозе глубоких вен (ТГВ) поражаются глубокие вены.
- К тромбообразованию предрасполагают три основных фактора: повреждение сосуда, стаз крови и гиперкоагуляция (триада Вирхова).
- повреждение сосуда может развиться при хирургическом вмешательстве (особенно при ортопедических, торакальных, абдоминальных и урологических операциях), травме (например, при переломах крупных костей), установке центрального венозного катетера.
- стазу крови способствуют обездвиженность (например, при длительных путешествиях, после хирургических вмешательств), отеки (например, при сердечной недостаточности).
- гиперкоагуляция развивается при беременности, злокачественных новообразованиях (особенно при опухолях поджелудочной железы, легких и молочной железы) и некоторых других состояниях (например, при приеме эстрогенов, антифосфолипидном синдроме, дефиците С-реактивного белка и протеина S).
Дифференциальный диагноз
- Целлюлит.
- Травма / кровоизлияние в мышцы.
- Разрыв подколенной кисты.
- Лимфостаз (лимфедема).
- Артриты, тендиниты.
- Постфлебитический синдром (расширение вены вследствие разрушения венозных клапанов в результате предшествующего тромбоза глубоких вен — наблюдается в 60% случаев тромбоза глубоких вен).
- Сердечная недостаточность.
- Нефротический синдром.
- Цирроз печени.
- Гипоальбуминемия.
Симптоматика
- Поверхностный венозный тромбоз: набухание, эритема, и увеличение кожной температуры в области пораженного участка вены. Пальпаторно — лентовидное (иногда болезненное) уплотнение по ходу вены.
- Тромбоз глубоких вен:
- может протекать бессимптомно.
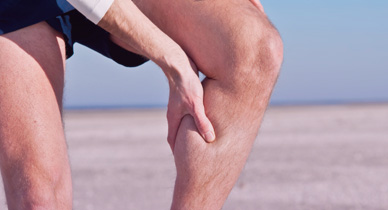
- асимметричный отек конечности, эритема, увеличение кожной температуры, напряжение мышц.
- расширение венозных коллатералей.
- phlegmasia cerulea dolens (цианоз конечности вследствие увеличения экстракции кислорода тканями).
- phlegmasia alba dolens (бледность конечности вследствие увеличения интерстициального давления и механического сдавления сосудов).
Диагностика
- Поверхностный венозный тромбоз: для правильной диагностики обычно бывает достаточно физикального исследования; другие методы исследования применяются для исключения сопутствующего тромбоза глубоких вен.
- Тромбоз глубоких вен:
- физикальное исследование малоинформативно.
- дуплексная ультрасонография вен высокочувствительна и специфична в отношении выявления тромбоза глубоких вен проксимальных участков вен, однако менее чувствительна для тромбоза глубоких вен вен голени (если у пациента с симптоматикой тромбоза глубоких вен ультрасонография имеет негативный результат, исследование необходимо повторить через 5-7 дней).
- EUSA D-димер является чувствительным (80%), но неспецифичным признаком тромбоза глубоких вен; самостоятельного значения для диагностики тромбоза глубоких вен не имеет.
- МРТ позволяет диагностировать тромбоз верхней и нижней полых вен, вен таза.
- рентгеноконтрастная венография в настоящее время используется редко в связи с инвазивностью.
- у лиц с тромбозом глубоких вен, не имеющих в анамнезе хирургических вмешательств или очевидных факторов риска, требуется исследование коагуляции.
- Поверхностный венозный тромбоз.
- приподнятое положение конечности, тепловые компрессы, НПВП (нестероидные противовоспалительные препараты) при наличии боли.
- если тромбоз локализуется вблизи устьев глубоких вен, подумайте о назначении антикоагулянтов
- Тромбоз глубоких вен: для предотвращения нарастания тромбоза и ТЭЛА (тромбоэмболии лёгочной артерии) необходима системная ант.икоагулянтная терапия.
- начните внутривенное введение простого гепарина или подкожное введение низкомолекулярных гепаринов.
- параллельно может быть начата терапия варфарином.
- прекратите гепаринотерапию через 48 ч после того, как МНО достигнет 2,0 (прием варфарина транзиторно усиливает коагуляцию, поэтому до истечения этого срока гипокоагуляция не достигнута).
- при первичном идиопатическом тромбозе глубоких вен или при тромбозе глубоких вен, имеющем установленную причину, терапию варфарином продолжайте 3-6 мес.
- неопределенно длительная терапия варфарином необходима при повторных идиопатических тромбозах глубоких вен или в тех случаях, когда сохраняются факторы риска этого заболевания (например, гиперкоагуляция).
- для предотвращения ТЭЛА в нижнюю полую вену может быть установлен кава-фильтр. Показаниями являются наличие противопоказаний к антикоагулянтной терапии, ее неэффективность (например, эпизод ТЭЛА, развившийся несмотря на адекватную антикоагулянтную терапию) или наличие других тяжелых заболеваний легких.
Важные замечания
- Поверхностный венозный тромбоз встречается часто и часто исчезает самостоятельно.
- Госпитализация не требуется; направьте пациента под временное амбулаторное наблюдение для исключения нарастания тромбоза.
- Тромбоз глубоких вен требует госпитализации при наличии тяжелой сопутствующей патологии, невозможности проведения амбулаторной антикоагулянтной терапии или ее контроля.
- В остальных случаях неосложненного тромбоза глубоких вен после подкожной инъекции низкомолекулярных гепаринов и назначения варфарина направьте пациента под тщательное амбулаторное наблюдение.
- Риск ТЭЛА при изолированном тромбозе глубоких вен вен голеней не увеличен и назначать антикоагулянты не требуется (повторите ультрасонографию через 5-7 дней для выявления распространения тромбоза глубоких вен, что потребует изменения тактики лечения).
Источники: http://www.4astniydom.ru/content/tromboz, http://studfiles.net/preview/6689517/page:9/, http://kindmed.ru/kardiologiya/133-venoznyy-tromboz.html